题目内容
17.已知25℃时,下列酸的电离常数:| 物质名称 | 醋酸 | 氢氰酸 | 氢氟酸 | 甲酸 |
| 电离常数K | 1.75×10-5 | 4.93×10-10 | 7.2×10-4 | 1.77×10-4 |
| A. | 醋酸 | B. | 氢氰酸 | C. | 氢氟酸 | D. | 甲酸 |
分析 由弱电解质的电离平衡常数可知,K越大,酸性越强,则等浓度时K越大,电离出c(H+)越大,以此来解答.
解答 解:由表格数据可知,氢氟酸的K最大,物质的量浓度均为0.1mol•L-1的上述溶液c(H+)最大的是氢氟酸,
故选C.
点评 本题考查弱电解质的电离,为高频考点,把握表格中数据、K与酸性的关系为解答的关键,侧重分析与应用能力的考查,注意K越大酸性越强,题目难度不大.

练习册系列答案
相关题目
5.下列物质中,主要成分属于硅酸盐的是( )
| A. | 烧碱 | B. | 玻璃 | C. | 石灰石 | D. | 胆矾 |
12.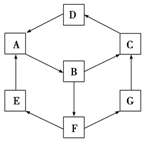 如图是无机物A~G在一定条件下的转化关系(部分产物及反应条件未列出).已知:①A、B、C、D、G含有同种元素.
如图是无机物A~G在一定条件下的转化关系(部分产物及反应条件未列出).已知:①A、B、C、D、G含有同种元素.
②
③E是通常情况下密度最小的气体;B与硝酸银溶液反应生成不溶于稀硝酸的白色沉淀;B也能将一种氧化物氧化为F,F是含有三种元素的化合物,稀的F溶液与A反应生成E、G.
根据以上信息填空:
(1)写出D的化学式:Fe2O3.
(2)G生成C的过程中所出现的现象为先产生白色沉淀,逐渐变为灰绿色,最后变为红褐色.
(3)写出下列反应的化学方程式:
E→A4H2+Fe3O4$\frac{\underline{\;高温\;}}{\;}$3Fe+4H2O;
A→B2Fe+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2FeCl3.
(4)B→F的离子方程式为;G与次氯酸反应的离子方程式为H++2Fe2++HClO═2Fe3++Cl-+H2O.
 如图是无机物A~G在一定条件下的转化关系(部分产物及反应条件未列出).已知:①A、B、C、D、G含有同种元素.
如图是无机物A~G在一定条件下的转化关系(部分产物及反应条件未列出).已知:①A、B、C、D、G含有同种元素.②
| 物质 | 纯A(单质) | B溶液 | C固体 | D固体 | G溶液 |
| 颜色 | 银白色 | 黄色 | 红褐色 | 红棕色 | 浅绿色 |
根据以上信息填空:
(1)写出D的化学式:Fe2O3.
(2)G生成C的过程中所出现的现象为先产生白色沉淀,逐渐变为灰绿色,最后变为红褐色.
(3)写出下列反应的化学方程式:
E→A4H2+Fe3O4$\frac{\underline{\;高温\;}}{\;}$3Fe+4H2O;
A→B2Fe+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2FeCl3.
(4)B→F的离子方程式为;G与次氯酸反应的离子方程式为H++2Fe2++HClO═2Fe3++Cl-+H2O.
2.下列有关说法不正确的是( )
| A. | 除去镁粉中混有的少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤 | |
| B. | 用明矾净水是因为Al3+水解生成的胶状Al(OH)3具有很强的吸附性 | |
| C. | 在相同浓度的盐酸中,纯铁比含碳量较高的生铁反应速率快 | |
| D. | 冶金工业中可以利用铝热反应原理冶炼钒、铬、锰等金属 |
6.下列有关NaClO2和NaCl混合溶液的叙述正确的是( )
| A. | 该溶液中,Fe2+、NH4+、SO42-、S2-可以大量共存 | |
| B. | 该溶液中,H+、K+、NO3-、SO42-可以大量共存 | |
| C. | 向该溶液中滴入少量FeSO4溶液,反应的离子方程式为:2Fe2++ClO-+2H+═Cl-+2Fe3++H2O | |
| D. | 向该溶液中加入浓硫酸,反应的离子方程式为:ClO2-+4H++3 Cl-=2Cl2↑+2 H2O |
7.在一定条件下,将3mol A和1mol B两种气体混合于固定容积为2L的密闭容器中,发生如下反应:3A (g)+B(s)?xH(g)+2G(g),2min末该反应达到平衡,生成0.8mol G,并测得H的浓度为0.2mol•L-1.下列判断正确的是( )
| A. | x=2 | |
| B. | 2 min内A的反应速率为0.3 mol•(L•min)-1 | |
| C. | 维持其他条件不变,将该混合物转移到固定容积为1 L的密闭容器中,再次平衡后H的浓度将大于0.4 mol•L-1 | |
| D. | 维持其他条件不变,再向容器中加入足量物质 A,最终H的浓度将达到0.5 mol•L-1 |
 ;
;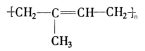 其单体的结构简式CH2=C(CH3)CH=CH2;
其单体的结构简式CH2=C(CH3)CH=CH2;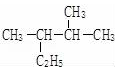 的名称(系统命名法)2,3-二甲基戊烷.
的名称(系统命名法)2,3-二甲基戊烷.
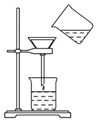 将含有少量氯化钾的硝酸钾固体提纯,某学生进行如图所示实验操作.回答下列问题:
将含有少量氯化钾的硝酸钾固体提纯,某学生进行如图所示实验操作.回答下列问题: