题目内容
11.下列各种情况下一定能大量共存的离子组为( )| A. | 向某无色溶液中加入铁粉能产生大量H2,则该溶液中存在大量Na+、Ca2+、C1-、NO3- | |
| B. | 水电离出的c(H+)=1×10-3mol•L-1的水溶液中Na+、CO32-、Cl-、K+ | |
| C. | pH=1的水溶液中NH4+、Cl-、Mg2+、SO42- | |
| D. | Al3+、HCO3-、I-、Ca2+ |
分析 A、加入铁粉能放出H2的溶液呈酸性;
B、水电离出的c(H+)=1×10-3mol•L-1,说明水的电离受促进,溶液中含弱离子碳酸根离子;
C、pH=1的水溶液是酸性溶液;
D、Al3+和HCO3-发生双水解,而不能共存.
解答 解:A、加入铁粉能放出H2的溶液呈酸性,酸性条件下NO3-不能大量存在,故A错误;
B、水电离出的c(H+)=1×10-3mol•L-1,说明水的电离受促进,溶液中含弱离子碳酸根离子,而CO32-与Na+、Cl-、K+能大量共存,故B正确;
C、pH=1的水溶液是酸性溶液,NH4+、Cl-、Mg2+、SO42-与氢离子能大量共存,故C正确;
D、Al3+和HCO3-发生双水解,生成氢氧化铝和二氧化碳气体,而不能共存,故D错误;
故选BC.
点评 本题考查离子共存,涉及常见离子的性质的考查,侧重于基础知识的综合运用,易错点为D,注意离子之间发生互促水解的性质,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
1.某同学在实验室研究Na2CO3和NaHCO3的性质及相互转化.
(1)分别向浓度均为0.1mol/LNa2CO3及NaHCO3溶液中滴加几滴酚酞试剂:
①Na2CO3溶液由无色变为红色,其原因是CO32-+H2O?HCO3-+OH-.
②NaHCO3溶液也由无色变为红色,其原因是HCO3-+H2O?H2CO3+OH-,HCO3-?H++CO32-,水解程度大于电离程度.
③比较两份溶液的颜色,红色较浅的是NaHCO3(填化学式).
(2)研究NaHCO3与CaCl2的反应.
①实验1中没有出现白色浑浊的原因是HCO3-浓度低,电离出的CO32-浓度更低,导致c(Ca2+)•c(CO32-)<Ksp(CaCO3).
②实验2中形成的分散系属于胶体.
③用离子方程式表示实验2中发生的反应Ca2++2HCO3-=CaCO3↓+CO2+H2O.
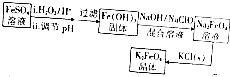
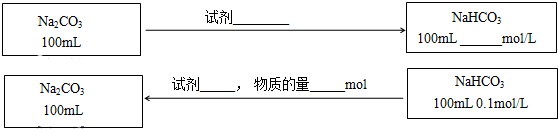
(3)在不引入其他杂质的前提下,实现Na2CO3与NaHCO3之间的转化,请在图中标出所用的试剂、用量或物质的浓度(反应前后溶液体积的变化可忽略).
(1)分别向浓度均为0.1mol/LNa2CO3及NaHCO3溶液中滴加几滴酚酞试剂:
①Na2CO3溶液由无色变为红色,其原因是CO32-+H2O?HCO3-+OH-.
②NaHCO3溶液也由无色变为红色,其原因是HCO3-+H2O?H2CO3+OH-,HCO3-?H++CO32-,水解程度大于电离程度.
③比较两份溶液的颜色,红色较浅的是NaHCO3(填化学式).
(2)研究NaHCO3与CaCl2的反应.
| 实验序号 | 实验操作 | 实验现象 |
| 实验1 | 向2mL 0.001mol/L NaHCO3溶液中加入1mL 0.1mol/LCaCl2溶液 | 无明显变化.用激光笔照射,没有出现光亮的通路. |
| 实验2 | 向2mL 0.1mol/L NaHCO3溶液中加入1mL 0.1mol/LCaCl2溶液 | 略显白色均匀的浑浊,用激光笔照射,出现光亮的通路. |
②实验2中形成的分散系属于胶体.
③用离子方程式表示实验2中发生的反应Ca2++2HCO3-=CaCO3↓+CO2+H2O.
(3)在不引入其他杂质的前提下,实现Na2CO3与NaHCO3之间的转化,请在图中标出所用的试剂、用量或物质的浓度(反应前后溶液体积的变化可忽略).

19.在强酸或强碱溶液中都可以大量共存的一组离子是( )
| A. | Na+、SO42-、Cl-、NO3- | B. | Na+、HCO3-、Ca2+、Cl- | ||
| C. | Na+、Cl-、NO3-、Fe3+ | D. | K+、Cl、CO32-、NO3- |
4.下列说法正确的是( )
| A. | 利用外接直流电源保护铁质建筑物,属于电化学中牺牲阳极的阴极保护法 | |
| B. | 科学仪器的使用利于我们认识物质的微观世界,现在人们借助扫描隧道显微镜,应用SMT技术可以“看”到越来越细微的结构,并实现对原子或分子的操纵 | |
| C. | 人们通常用标准燃烧热或热值来衡量燃料燃烧放出热量的大小,某物质的热值越高则其标准燃烧热越大 | |
| D. | 汽车尾气催化转化装置可将尾气中的NO和CO等有害气体转化为N2和CO2,该装置中的催化剂可降低NO和CO反应的活化能,加快该反应的速率,同时能提高该反应的平衡转化率 |
8.下列四个图象的有关描述错误的是( )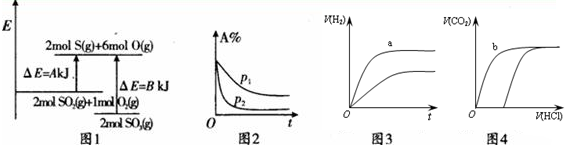
注:△E:表示能量,p表示压强;t表示时间,V表示体积,%表示B的体积百分含量.

注:△E:表示能量,p表示压强;t表示时间,V表示体积,%表示B的体积百分含量.
| A. | 图1表示化学反应2S02(g)+O2(g)?2S03(g)的能量变化,该反应的△H=A一BkJ/mol | |
| B. | 图2表示其他条件不变时,反应2A(g)+B(g)?c(g)+D(g)在不同压强下随时间的变化 | |
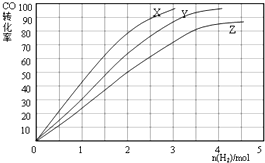
| C. | 图3表示体积和浓度均相同的HCl和CH3COOH两种溶液中,分别加入足量的锌,产生H2的体积随时间的变化,则a表示CH3COOH溶液 | |
| D. | 图4表示100 ml O.1 mol•L-Na2C03和NaHC03两种溶液中,分别逐滴滴加0.1 mol•L-1HCl,产生CO2 的体积随盐酸体积的变化,则b表示NaHCO3溶液 |
9.25℃时,浓度均为0.1mol•L-1的HA溶液和BOH溶液,pH分别是1和11.下列说法正确的是( )
| A. | 在0.1 mol•L-1BA溶液中c(A-)+c(H+)=c(BOH)+c(OH-) | |
| B. | 若将0.1 mol•L-1BOH溶液稀释至0.001 mol•L-1则溶液的pH=9 | |
| C. | 若将一定量的上述两溶液混合后pH=7,则混合液中:c(A-)>c(B+) | |
| D. | 若将上述两溶液按体积比1:2混合,则混合液中:c(B+)>c(A-)>c(OH-)>c(H+) |