题目内容
12.下列混合物中,用分液漏斗不能分离的是( )| A. | 酒精和水 | B. | 汽油和水 | C. | 苯和水 | D. | 四氯化碳和水 |
分析 两种液体互不相溶,混合时分层,则可利用分液漏斗分离,若液体相互溶解不能利用分液漏斗分离,以此来解答.
解答 解:酒精易溶于水,不分层,不能用分液漏斗分离.而汽油、苯、四氯化碳都不溶于水,形成上下两层,可用分液漏斗分离.
故选A.
点评 本题考查混合物的分离,为高频考点,侧重于学生的分析能力的和实验能力的考查,明确物质的溶解性及能利用分液漏斗分离的混合物满足分层的条件即可解答,题目难度不大.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
3.根据硫元素的原子结构,推测硫元素的最高正价和最低负价分别为( )
| A. | +2、-2 | B. | +6、-2 | C. | +4、-4 | D. | +2、-6 |
7.有些化学反应不仅与反应物种类有关,还与反应条件(反应温度、反应物浓度)或反应物物质的量的比值有关,下列反应中不随反应条件(反应温度、反应物浓度)、反应物物质的量的而变化的是( )
| A. | 氯气与铁粉 | B. | 二氧化碳与石灰水 | ||
| C. | 锌与硫酸 | D. | 碳酸钠与硫酸 |
17.下列离子方程式书写正确的是( )
| A. | 铝粉投入到冷浓硝酸中:2Al+6H+=2Al3++3H2↑ | |
| B. | 铁与盐酸反应:2Fe+6H+=2Fe3++3H2↑ | |
| C. | 用小苏打治疗胃酸过多:H++HCO3-=H2O+CO2↑ | |
| D. | Ba(OH)2与稀H2SO4反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
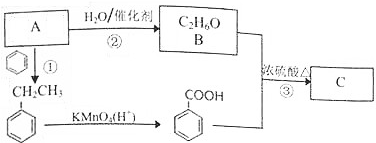
 +CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$
+CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$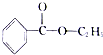 +H2O.
+H2O.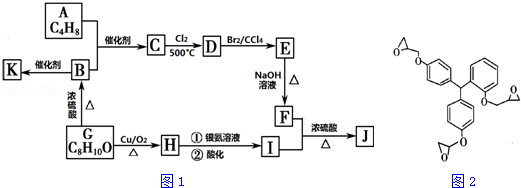
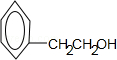 .
. ;F+I→J
;F+I→J .
.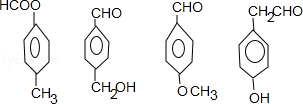 .
.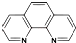 ),它能与Fe2+形成红色配合物(如图甲),该配离子中Fe2+与氮原子形成配位键共有6个.
),它能与Fe2+形成红色配合物(如图甲),该配离子中Fe2+与氮原子形成配位键共有6个.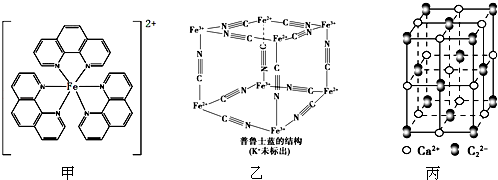
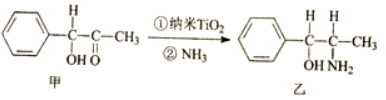
 ,其中σ键与π键数目之比为1:2.
,其中σ键与π键数目之比为1:2.