题目内容
5.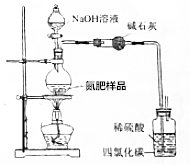 用如图所示装置测定氮肥[NH4HCO3中含(NH4)2CO3]中NH4HCO3的质量分数(不考虑铵盐溶液分解).
用如图所示装置测定氮肥[NH4HCO3中含(NH4)2CO3]中NH4HCO3的质量分数(不考虑铵盐溶液分解).(1)实验时,若需配制100mL5.0mol•L-1的NaOH溶液,则所需NaOH固体的质量为20.0g.
(2)为提高实验的准确性,待充分反应后需继续向烧瓶中鼓入空气一段时间,其目的是把生成的氨气全部带入浓硫酸中吸收.
(3)取7.59g样品与NaOH溶液混合,完全溶解后,加热充分反应,并使生成的氨气被稀硫酸吸收,测得稀硫酸增重1.7g.
①样品中NH4+的物质的量为0.1mol.
②NH4HCO3的质量分数93.7%.
分析 (1)根据n=cV计算NaOH的物质的量,再根据m=nM计算NaOH的质量;
(2)待充分反应后需继续向烧瓶中鼓入空气一段时间是利用空气把生成的氨气全部带入浓硫酸中吸收;
(3)浓硫酸中增重的质量为生成氨气的质量,计算得到铵根离子的物质的量结合以上守恒列方程计算样品中碳酸氢铵的质量得到质量分数.
解答 解:(1)n(NaOH)=0.1L×5.0mol/L=0.5mol,则m(NaOH)=0.5mol×40g/mol=20.0g,
故答案为:20.0g;
(2)为提高实验的准确性,待充分反应后需继续向烧瓶中鼓入空气一段时间,其目的是:把生成的氨气全部带入浓硫酸中吸收,
故答案为:把生成的氨气全部带入浓硫酸中吸收;
(3)取7.59g样品与NaOH溶液混合,完全溶解后,加热充分反应,并使生成的氨气被稀硫酸吸收,测得稀硫酸增重1.7g,增重为氨气质量,
①氮元素守恒得到铵根离子物质的量=氨气物质的量=$\frac{1.7g}{17g/mol}$=0.1mol,故答案为:0.1;
②NH4HCO3中含(NH4)2CO3,设碳酸氢铵物质的量为x,碳酸氨物质的量为y,则
79x+96y=7.59g
x+2y=0.1
x=0.09mol
y=0.005mol
NH4HCO3的质量分数=$\frac{0.09mol×79g/mol}{7.59g}$×100%=93.7%,
故答案为:93.7%.
点评 本题考查了混合物含量的实验测定方法、实验方案的设计理解、定量计算等,掌握基础是解题关键,题目难度中等.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
15.关于Cl-和Cl2的说法正确的是( )
| A. | 都能与Fe反应生成FeCl3 | B. | 与AgNO3溶液反应都生成白色沉淀 | ||
| C. | 均有毒 | D. | 都具有氧化性 |
16.在生产过程中,除去铁制品上的铁锈,可先用下列溶液洗涤的是( )
| A. | NaOH | B. | CuSO4 | C. | HCl | D. | NaCl |
10.向氯化亚铁溶液中加入过量的氨水,有沉淀生成.过滤.加热沉淀物至质量不再发声变化,得到红棕色的残渣.上述沉淀和残渣分别为( )
| A. | Fe(OH)2、Fe(OH)3;Fe3O4 | B. | Fe(OH)2;FeO | ||
| C. | Fe(OH)2、Fe(OH)3;Fe2O3 | D. | Fe2O3;Fe(OH)3 |
17.下列离子方程式中,正确的是( )
| A. | 氢氧化钠溶液中通入过量CO2:CO2+2OH-═CO${\;}_{3}^{2-}$+H2O | |
| B. | 向澄清石灰水中通入过量CO2;Ca2++2OH-+CO2=CaCO3↓++H2O | |
| C. | 硫酸氢钠溶液中加入过量氢氧化钡溶液:2HSO${\;}_{4}^{-}$+2Ba2++2OH-=2BaSO4↓+2H2O | |
| D. | 向碳酸氢钙溶液中加入过量石灰水:Ca2++OH-+HCO${\;}_{3}^{-}$=CaCO3↓+H2O |