题目内容
将15ml 2mol/LNa2CO3的溶液逐滴加入到40ml 0.5mol/LMCln的盐溶液中,恰好将溶液中的Mn+离子完全沉淀为碳酸盐,则MCln中的n值是
A.3 B.4 C.2 D.1
A
【解析】
试题解析:Na2CO3溶液中CO32-的物质的量为15mL×10-3×2mol/L=0.03mol,MCln盐溶液中Mn+离子的物质的量为40mL×10-3×0.5mol/L=0.02mol,由反应中恰好将溶液中的Mn+离子完全沉淀为碳酸盐,及M的化合价为+n,则Na2CO3与MCln反应对应的关系式为:
2Mn+ ~ nCO32-
2 n
0.02mol 0.03mol
 =
=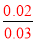 ,解得n=3。
,解得n=3。
考点:离子反应的计算

练习册系列答案
相关题目
 H2↑+Cl2↑+ 2OH-
H2↑+Cl2↑+ 2OH-


 、
、 、
、 、
、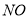 、
、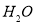 。则该反应中还原产物是______ ;若反应过程中转移了0.3
。则该反应中还原产物是______ ;若反应过程中转移了0.3 电子,则氧化产物的质量_____
电子,则氧化产物的质量_____ 。
。 Al(OH)4― + H+ ;②NH3+H2O
Al(OH)4― + H+ ;②NH3+H2O