��Ŀ����
4���о�NOx��SO2��CO�ȴ�����Ⱦ����Ĵ�������������Ҫ���壮��1��NOx������β���е���Ҫ��Ⱦ��֮һ�� NOx���γ����꣬д��NO2ת��ΪHNO3�Ļ�ѧ����ʽ��3NO2+H2O=2HNO3+NO��
��2��������CO��SO2�̵�����Ⱦ��һ�ַ����ǽ����ڴ���������ת��Ϊ����S����֪��
��CO��g��+$\frac{1}{2}$O2��g���TCO2��g����H=-283.0kJ•mol-1��
��S��s��+O2��g���TSO2��g����H=-296.0kJ•mol-1��
�˷�Ӧ���Ȼ�ѧ����ʽ��2CO��g��+SO2��g��=S��s��+2CO2��g����H1=-270KJ•mol-1��
��3��������������ɹ⻯ѧ�����ͳ�������ĵ���Ҫ���壮��֪��
��CO��g��+NO2��g���TNO��g��+CO2��g����H=-a kJ•mol-1��a��0��
��2CO��g��+2NO��g���TN2��g��+2CO2��g����H=-b kJ•mol-1��b��0��
���ñ�״���� 3.36L CO��ԭNO2��N2��CO��ȫ��Ӧ��������������ת�Ƶ��ӵ���ĿΪ0.3NA���ų�������Ϊ$\frac{3��2a+b��}{80}$kJ���ú���a��b�Ĵ���ʽ��ʾ����
��4����CH4����ԭNOxҲ�������������������Ⱦ�����磺
��CH4��g��+4NO2��g���T4NO��g��+CO2��g��+2H2O��g����H1=-574kJ•mol-1
��CH4��g��+4NO��g���T2N2��g��+CO2��g��+2H2O��g����H2=��
��1mol CH4��ԭNO2��N2���������зų�������Ϊ867kJ�����H2=-1160kJ/mol��
���� ��1������������ˮ��Ӧ���������һ��������
��2�����ø�˹���ɽ�����ʽ�١�2-�ڵ��Ȼ�ѧ����ʽ��
��3�����ݸ�˹�������4CO��g��+2NO2��g��=N2��g��+4CO2��g���ķ�Ӧ�ȣ���Ӧ��3.36LCO��0.15molת��0.3mol���ӣ��������ʵ���֮�ȵ�������������ų���������
��4��������ʽ��+�ڵ�2CH4��g��+4NO2��g��=2N2��g��+2CO2��g��+4H2O��g����H=��H1+��H2�����1molCH4��ԭNO2��N2�����������зų�������Ϊ867kJ���㣮
��� �⣺��1������������ˮ��Ӧ���������һ����������Ӧ����ʽΪ��3NO2+H2O=2HNO3+NO��
�ʴ�Ϊ��3NO2+H2O=2HNO3+NO��
��2����CO��g��+$\frac{1}{2}$O2��g��=CO2��g����H=-283.0kJ•mol-1
��S��s��+O2��g��=SO2��g����H=-296.0kJ•mol-1
������ʽ�١�2-�ڵ�2CO��g��+SO2��g��=S��s��+2CO2��g����H1=��-283.0KJ•mol-1����2-��-296.0KJ•mol-1��=-270kJ•mol-1��
�������Ȼ�ѧ��Ӧ����ʽΪ��2CO��g��+SO2��g��=S��s��+2CO2��g����H1=-270kJ•mol-1��
�ʴ�Ϊ��2CO��g��+SO2��g��=S��s��+2CO2��g����H1=-270kJ•mol-1��
��3����CO��g��+NO2��g��=NO��g��+CO2��g����H=-a kJ•mol-1��a��0��
��2CO��g��+2NO ��g��=N2��g��+2CO2��g����H=-b kJ•mol-1��b��0��
������ʽ�١�2+�ڵ�4CO��g��+2NO2��g��=N2��g��+4CO2��g����H=��-a�� KJ•mol-1��2+��-b KJ•mol-1��=-��2a+b��kJ•mol-1
�������Ȼ�ѧ��Ӧ����ʽΪ��4CO��g��+2NO2��g��=N2��g��+4CO2��g����H=-��2a+b��kJ•mol-1��
���ݷ���ʽ֪ת�Ƶ��ӵ����ʵ���Ϊ$\frac{3.36L}{22.4L/mol}$��2=0.3mol��������ĿΪ0.3NA���ų�������Ϊ$\frac{3.36L}{22.4L/mol}$��$\frac{2a+b}{4}$kJ•mol-1=$\frac{3��2a+b��}{80}$kJ��
�ʴ�Ϊ��0.3NA��$\frac{3��2a+b��}{80}$��
��4����CH4��g��+4NO2��g��=4NO��g��+CO2��g��+2H2O��g����H1=-574kJ•mol-1
��CH4��g��+4NO��g��=2N2��g��+CO2��g��+2H2O��g����H2=��
������ʽ��+�ڵ�2CH4��g��+4NO2��g��=2N2��g��+2CO2��g��+4H2O��g����H=��H1+��H2��
���ݷ���ʽ֪��1mol CH4��ԭNO2��N2���������зų�������Ϊ867kJ�����ԡ�H2=-867kJ/mol��2-��-574kJ/mol��=-1160kJ/mol��
�ʴ�Ϊ��-1160kJ/mol��
���� ���⿼���˸�˹���ɵ��йؼ��㣬�漰��ѧ��Ӧ����ʽ���Ȼ�ѧ��Ӧ����ʽ����д��֪ʶ�㣬�����ø�˹������д����Ӧ��֮��Ĺ�ϵʽ�ǽⱾ��ؼ����ѶȲ���

| A�� | ������С�����ƽ�������ƶ����ٴδ�ƽ��ʱ��ɫ��ԭƽ��dz | |
| B�� | �������£��淴Ӧ���ʼӿ죬����Ӧ���ʼ��� | |
| C�� | ���ı�����ʹƽ�������ƶ�����÷�Ӧ��ƽ�ⳣ�������� | |
| D�� | ���º��ݣ���������NO2���ٴδ�ƽ��ʱNO2��ת���ʱ�ԭƽ��Ĵ� |
| A�� | �����ӵİ뾶��d��c | |
| B�� | ���ʵķе㣺a��b | |
| C�� | b��d���������Ӧ��ˮ�����Ϊǿ�� | |
| D�� | b��c���γ����ӻ�����b3c2 |
| ��ʵ | ���ۻ��Ʋ� | |
| A | Na����ˮ���ҷ�Ӧ������H2 | Mg���ˮѸ�ٷ�Ӧ������H2 |
| B | F2��H2�������һ��ϣ����ɵ�HF���ȶ� | I2��H2����Ҳ�ܻ��ϣ����ɵ�HIҲ���ȶ� |
| C | Na��O2���ȷ�Ӧ����Na2O2 | IAԪ�ص�����O2���ȷ�Ӧ�����ɹ������� |
| D | H3PO4����ǿ�ᣬAs��P��ͬ����ǽ���Ԫ�� | H3AsO4��ǿ�� |
| A�� | A | B�� | B | C�� | C | D�� | D |
| A�� | ȡ�÷�ĩ״��������С����ʱ��Ӧ��ҩ��ֽ�ۣ�ȡ�ÿ�״����ʱ��Ӧ�����Ӽ�ȡ | |
| B�� | ȡ��ϸ��ƿ�����Һʱ��������ƿ�������������ϣ�Ȼ���ǩ��������ƿ�ӣ�ƿ��Ҫ�������Թܿڣ���Һ�建���ص����Թ� | |
| C�� | ��ͷ�ι�ȡ��һ����Һ��ֱ��ȡ��һ�ֲ����䷴Ӧ����Һ | |
| D�� | ��ijʵ��û��ȷ��ҩƷ����˵��ʱ��Ϊ������������ȡ��ҩƷԽ��Խ�� |
NO��g��+H2��g��=$\frac{1}{2}$N2��g��+H2O��g���ġ�HΪ��������
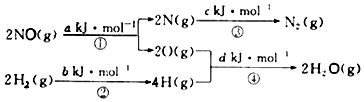
| A�� | 0.5��a+b-c-d��kJ/mol | B�� | 0.5��c+a-d-b��kJ/mol | ||
| C�� | 0.5��c+d-a-b��kJ/mol | D�� | 0.5��c+d-a-b��kJ/mol |