题目内容
50℃时,下列各溶液中,离子的物质的量浓度关系正确的是C( )
| A、pH=4的醋酸中:c(H+)=4.0mol?L-1 |
| B、pH=12的纯碱溶液中:c(OH-)=1.0×10-2mol?L-1 |
| C、饱和食盐水中:c(Na+)+c(H+)=c(Cl-)+c(OH-) |
| D、饱和小苏打溶液中:c(Na+)=c(HCO3-) |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:A.c(H+)=10-pHmol/L;
B.据pH和水的离子积常数计算氢氧根离子浓度;
C.任何电解质溶液中都存在电荷守恒,根据电荷守恒判断;
D.任何电解质溶液中都存在物料守恒,根据物料守恒判断.
B.据pH和水的离子积常数计算氢氧根离子浓度;
C.任何电解质溶液中都存在电荷守恒,根据电荷守恒判断;
D.任何电解质溶液中都存在物料守恒,根据物料守恒判断.
解答:
解:A.c(H+)=10-pHmol/L=10-4mol/L,故A错误;
B.pH=12,c(H+)=10-pHmol/L=10-12mol/L所以室温时c(OH-)=
mol/L=1.0×10-2mol?L-1,50℃时,c(OH-)>1.0×10-2mol?L-1,故B错误;
C.任何电解质溶液中都存在电荷守恒,根据电荷守恒得c(Na+)+c(H+)=c(Cl-)+c(OH-),故C正确;
D.小苏打是碳酸氢钠,碳酸氢钠溶液中存在物料守恒,根据物料守恒得c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3),故D错误;
故选C.
B.pH=12,c(H+)=10-pHmol/L=10-12mol/L所以室温时c(OH-)=
| 10-14 |
| 10-12 |
C.任何电解质溶液中都存在电荷守恒,根据电荷守恒得c(Na+)+c(H+)=c(Cl-)+c(OH-),故C正确;
D.小苏打是碳酸氢钠,碳酸氢钠溶液中存在物料守恒,根据物料守恒得c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3),故D错误;
故选C.
点评:本题考查了离子浓度大小的比较,根据溶液中溶质的性质结合电荷守恒和物料守恒分析解答,易错选项是D,注意该温度不是室温,水的离子积常数不是10-14,为易错点.

练习册系列答案
 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
某强酸性溶液中含有大量的Fe2+和Ba2+,则下列离子可与该溶液大量共存的是( )
| A、SO42- |
| B、Cl- |
| C、CO32- |
| D、NO3- |
一定温度下,将2molX和1molY通入体积为1L的密闭容器中,发生反应2X(g)+Y(g)?2Z(g)△H<0,其中Z的浓度随时间变化的数据如下表所示:
下列说法不正确的是( )
| 时间 | 0min | 2min | 4min | 6min | 8min | 10min |
| Z的浓度mol/L | 0 | 0.8 | 1.2 | 1.4 | 1.4 | 1.4 |
| A、用Y来表示0-4min的平均反应速率为0.15mol/(L?min) |
| B、该温度下反应的化学平衡常数为18.15 |
| C、向平衡体系中再加入2molX和1mol Y,达到新的平衡时X的体积分数增大 |
| D、对平衡体系降低温度,化学反应后速率减慢,但Y的转化率增大 |
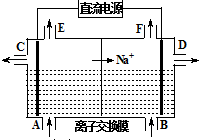 电解原理在工业生产中有广泛的应用.
电解原理在工业生产中有广泛的应用.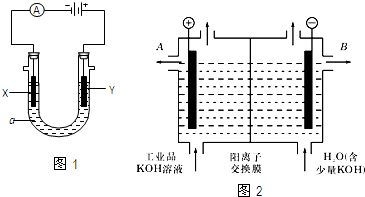
 如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.
如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.
 某兴趣小组利用如图装置,将不同浓度的硫酸与3mL 无水乙醇和2mL 冰醋酸混合,分别进行制取乙酸乙酯的研究.
某兴趣小组利用如图装置,将不同浓度的硫酸与3mL 无水乙醇和2mL 冰醋酸混合,分别进行制取乙酸乙酯的研究.