题目内容
在NaOH溶液中通入少量CO2时,发生反应2NaOH+CO2═Na2CO3+H2O,在NaOH溶液中通入过量CO2时,发生反应NaOH+CO2=NaHCO3,现在用1L 1.0mol/L 的NaOH溶液吸收0.8moL CO2,则所得溶液中Na2CO3和NaHCO3的物质的量的比是多少?
考点:有关混合物反应的计算
专题:
分析:根据n=cV计算出氢氧化钠的物质的量,根据反应方程式2NaOH+CO2═Na2CO3+H2O、NaOH+CO2=NaHCO3判断过量情况及反应产物,然后设出未知数计算出Na2CO3和NaHCO3的物质的量的比即可.
解答:
解:1L 1.0mol/L 的NaOH溶液中含有氢氧化钠的物质的量为:1mol/L×1L=1mol,根据2NaOH+CO2═Na2CO3+H2O可知,如果完全反应生成碳酸钠,需要消耗0.5mol二氧化碳,若生成碳酸氢钠:NaOH+CO2=NaHCO3,则消耗1mol二氧化碳,
所以二者反应生成碳酸钠和碳酸氢钠的混合物,
设反应生成碳酸钠xmol、碳酸氢钠ymol,
则:2x+y=1mol、x+y=0.8mol,
解得:x=0.2mol、y=0.6mol,
则则所得溶液中Na2CO3和NaHCO3的物质的量的比为:0.2mol:0.6mol=1:3,
答:所得溶液中Na2CO3和NaHCO3的物质的量的比为1:3.
所以二者反应生成碳酸钠和碳酸氢钠的混合物,
设反应生成碳酸钠xmol、碳酸氢钠ymol,
则:2x+y=1mol、x+y=0.8mol,
解得:x=0.2mol、y=0.6mol,
则则所得溶液中Na2CO3和NaHCO3的物质的量的比为:0.2mol:0.6mol=1:3,
答:所得溶液中Na2CO3和NaHCO3的物质的量的比为1:3.
点评:本题考查了化学方程式的计算,题目难度不大,注意根据反应物的物质的量先判断过量情况,从而得出反应产物,然后根据质量守恒定律列式计算,试题培养了学生的分析、理解能力.

练习册系列答案
相关题目
去除氧化膜的镁条插入盛有少量饱和FeCl3溶液的试管中,片刻后大量反应液涌向试管中,反应液呈现深红棕色,并有大量的红褐色固体物质,取出镁条、冲洗,发现镁条表面完全变黑,靠近磁铁,镁条立即被吸起来.依据上述实验现象的推论不正确的是( )
| A、Fe3+比H+的氧化性强,故镁将Fe3+还原完全后再与H+反应 |
| B、镁和生成的铁构成许多微型原电池,故反应剧烈 |
| C、反应放热温度升高,故反应剧烈 |
| D、反应产物含有Fe(OH)3、Fe、H2 |
下列各组中的两种有机物互为同系物的是( )
| A、乙醇和二甲醚(CH3-O-CH3) |
| B、CH3COOH和硬脂酸(C17H35COOH) |
| C、乙烷和乙烯 |
| D、淀粉和纤维素 |
下列描述正确的是( )
| A、氯气、活性炭都能使品红溶液褪色,它们的漂白原理相同 |
| B、滴加石蕊试液显红色的溶液:Fe3+、NH4+、I-可能大量共存 |
| C、某溶液中加入盐酸酸化的氯化钡产生白色沉淀,原溶液中一定含有SO42- |
| D、Fe(N03)2溶液中滴加少量稀硫酸会变黄色 |
下列有关金属及其化合物的说法中,错误的是( )
| A、生活中用碱液洗涤铝制饮具 |
| B、铁、铜制品要保持干燥,以防生锈 |
| C、用过氧化钠做潜水呼吸面具供氧剂 |
| D、用小苏打治疗胃酸过多 |
下列化学式中,能表示正长石(KAlSi3O8)的是( )
| A、K2O?Al2O3?3SiO2 |
| B、K2O?2Al2O3?3SiO2 |
| C、K2O?Al2O3?6SiO2 |
| D、2K2O?2Al2O3?6SiO2 |
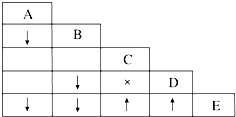 有五瓶损坏标签的试剂,分别盛有AgNO3溶液、稀硝酸、盐酸、BaCl2溶液、K2CO3溶液,为了确定各瓶中是什么试剂,将它们任意编号为A、B、C、D、E,用小试管各取少量,多次进行两两混合反应,反应现象如表所示.表中“↓”表示生成沉淀,“↑”表示生成气体,“×”表示没有明显现象,空格表示实验未做.
有五瓶损坏标签的试剂,分别盛有AgNO3溶液、稀硝酸、盐酸、BaCl2溶液、K2CO3溶液,为了确定各瓶中是什么试剂,将它们任意编号为A、B、C、D、E,用小试管各取少量,多次进行两两混合反应,反应现象如表所示.表中“↓”表示生成沉淀,“↑”表示生成气体,“×”表示没有明显现象,空格表示实验未做.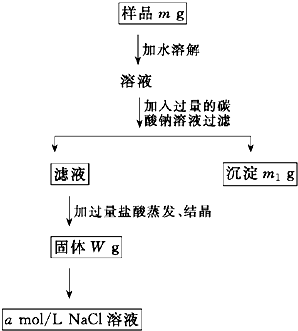 欲用含有少量氯化钙的氯化钠固体,配制100mL a mol/L的氯化钠溶液,设计了下面的操作方案.根据方案操作步骤回答下列问题:
欲用含有少量氯化钙的氯化钠固体,配制100mL a mol/L的氯化钠溶液,设计了下面的操作方案.根据方案操作步骤回答下列问题: