题目内容
1.下列说法正确的是(NA表示阿伏加德罗常数的值)( )| A. | 28 g氮气所含的原子数目为NA | |
| B. | 4 g金属钙变成离子时失去的电子数目为0.1NA | |
| C. | 22.4 L CH4的质量与NA个甲烷分子的质量之和相等 | |
| D. | 标准状况下,22.4 L CH4和氧气的混合物所含的分子数为NA |
分析 A.28g氮气是物质的量是1mol,含有2mol氮原子;
B.钙原子最外层2个电子;
C.气体摩尔体积标准状况下为22.4L/mol;
D.标准状况下气体摩尔体积为22.4L/mol.
解答 解:A.氮气分子是双原子的,28g氮气所含的原子数目为2NA,故A错误;
B.4g钙的物质的量为0.1mol,而钙的化合价为+2价,故0.1mol钙变为钙离子时失去0.2mol电子,故B错误;
C.温度压强不知,22.4 L CH4的物质的量不是1mol,故C错误;
D.标准状况下,22.4 L CH4和氧气的混合物物质的量=$\frac{22.4L}{22.4L/mol}$=1mol,所含的分子数为NA,故D正确;
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,题目难度不大.

练习册系列答案
相关题目
10.下列物质的水溶液因水解而呈酸性的是( )
| A. | NaHSO4 | B. | NH4Cl | C. | SO2 | D. | H2SO4 |
12.下列说法正确的是( )
| A. | 摩尔是国际科学界建议采用的一种物理量 | |
| B. | HNO3的摩尔质量是63g | |
| C. | 我们把含有6.02×1023个粒子的任何粒子的集体计量为1摩尔 | |
| D. | 1mol氧含6.02×1023个O2 |
9. 室温下,将1.000mol•L-1盐酸滴入20.00 mL 1.000mol•L-1的氨水中,溶液pH和温度随加入盐酸体积的变化曲线如图所示.下列有关说法中不正确的是( )
室温下,将1.000mol•L-1盐酸滴入20.00 mL 1.000mol•L-1的氨水中,溶液pH和温度随加入盐酸体积的变化曲线如图所示.下列有关说法中不正确的是( )
 室温下,将1.000mol•L-1盐酸滴入20.00 mL 1.000mol•L-1的氨水中,溶液pH和温度随加入盐酸体积的变化曲线如图所示.下列有关说法中不正确的是( )
室温下,将1.000mol•L-1盐酸滴入20.00 mL 1.000mol•L-1的氨水中,溶液pH和温度随加入盐酸体积的变化曲线如图所示.下列有关说法中不正确的是( )| A. | a点:由水电离出的c(H+)>1.0×10-14mol/L | |
| B. | b点:c(NH4+)+c(NH3•H2O)>c(Cl-) | |
| C. | c点:c(Cl-)<c(NH4+) | |
| D. | d点后,溶液温度略下降的主要原因是NH3•H2O电离吸热 |
13.下列叙述正确的是( )
| A. | 95℃纯水的pH<7,说明加热可导致水呈酸性 | |
| B. | pH=3的醋酸溶液稀释至10倍后pH=4 | |
| C. | 0.2 mol/L的盐酸与0.1 mol/L的盐酸等体积混合后pH=1.5 | |
| D. | 若向氨水中加入等浓度稀盐酸至溶液正好呈中性,则所用稀盐酸的体积一定小于氨水的体积 |
10.下列物质间不能发生离子反应的是( )
| A. | Na2SO4溶液与BaCl2溶液 | B. | NaOH溶液和稀H2SO4溶液 | ||
| C. | NaCl溶液与KNO3溶液 | D. | Na2CO3溶液与稀盐酸 |
11.按物质的组成进行分类,HNO3应属于①强酸;②氧化物;③含氧酸;④一元酸;⑤化合物( )
| A. | ①②③④⑤ | B. | ①③⑤ | C. | ①②③⑤ | D. | ①③④⑤ |
 .
.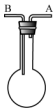 利用如图装置收集以下气体:①H2、②Cl2、③CH4、④HCl、⑤HBr
利用如图装置收集以下气体:①H2、②Cl2、③CH4、④HCl、⑤HBr