题目内容
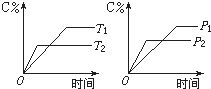 可逆反应mA(s)+nB(g)?pC(g)+qD(g)反应过程中,当其它条件不变时,C的质量分数与温度(T)和压强(P)的关系如图,根据图中曲线分析,判断下列叙述中正确的是( )
可逆反应mA(s)+nB(g)?pC(g)+qD(g)反应过程中,当其它条件不变时,C的质量分数与温度(T)和压强(P)的关系如图,根据图中曲线分析,判断下列叙述中正确的是( )| A、到达平衡后,若使用催化剂,C的质量分数增大 |
| B、平衡后,若升高温度,平衡则向逆反应方向移动 |
| C、平衡后,增大A的量,有利于平衡向正反应方向移动 |
| D、化学方程式中一定n>p+q |
考点:体积百分含量随温度、压强变化曲线
专题:化学平衡专题
分析:由左图知,升高温度,C%减小,则平衡向逆向移动,升高温度平衡向吸热反应移动,故正反应为放热反应;由右图可知,压强为P2先到达平衡,故P2>P1,增大压强,C%减小,则平衡向逆向移动,增大压强平衡向体积减小的方向移动,故n<p+q.
A、催化剂对化学平衡移动无影响.
B、由左图知,升高温度,C%减小,则平衡向逆向移动.
C、A为固体,对平衡无影响.
D、增大压强,C%减小,则平衡向逆向移动,增大压强平衡向体积减小的方向移动.
A、催化剂对化学平衡移动无影响.
B、由左图知,升高温度,C%减小,则平衡向逆向移动.
C、A为固体,对平衡无影响.
D、增大压强,C%减小,则平衡向逆向移动,增大压强平衡向体积减小的方向移动.
解答:
解:A、使用催化剂,缩短到达平衡时间,平衡不移动,C的质量分数不变,故A错误;
B、由左图知,升高温度,C%减小,则平衡向逆向移动,故B正确;
C、达平衡后增加A的量,因A为固体,对平衡无影响,故C错误;
D、增大压强,C%减小,则平衡向逆向移动,增大压强平衡向体积减小的方向移动,故n<p+q,故D错误.
故选:B.
B、由左图知,升高温度,C%减小,则平衡向逆向移动,故B正确;
C、达平衡后增加A的量,因A为固体,对平衡无影响,故C错误;
D、增大压强,C%减小,则平衡向逆向移动,增大压强平衡向体积减小的方向移动,故n<p+q,故D错误.
故选:B.
点评:图象的解题方法是“先拐先平”,即曲线先折拐的首先达到平衡,以此判断温度或压强的高低,再依据外界条件对平衡的影响确定答案.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
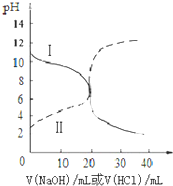 25℃时,取浓度均为0.1mol?L-1的醋酸溶液和氨水溶液各20mL,分别用浓度均为0.1mol?L-1NaOH溶液和盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如右图所示.下列说法不正确的是( )
25℃时,取浓度均为0.1mol?L-1的醋酸溶液和氨水溶液各20mL,分别用浓度均为0.1mol?L-1NaOH溶液和盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如右图所示.下列说法不正确的是( )| A、曲线Ⅰ:滴加溶液到20 mL时溶液的pH=5则:c(H+)-c((NH3?H2O)=c(OH-)=1×10-9 mol?L-1 |
| B、曲线Ⅰ:滴加溶液到20 mL时:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| C、曲线Ⅱ:滴加溶液在10 mL~20 mL之间存在:c(NH4+)=c(Cl-)>c(OH-)=c(H+) |
| D、曲线Ⅱ:滴加溶液到10 mL时:c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)] |
在体积为2L的恒容密闭容器中发生反应xA(g)+yB(g)?zC(g),图I表示200℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系.则下列结论正确的是( )


| A、若在图Ⅰ所示的平衡状态下,再向体系中充入He,重新达到平衡前v(正)>v(逆) |
| B、200℃时,反应从开始到刚好达平衡的平均速率v(B)=0.02 mol?L-1?min-1 |
| C、图Ⅱ所知反应xA(g)+yB(g)?zC(g)的△H<0 |
| D、200℃时,向容器中充入2 mol A 和1 mol B,达到平衡时,A 的体积分数大于0.5 |
 如图所示,是在其他条件一定时,反应2A+B?2C△H<0,A的最大转化率与温度关系曲线,下列叙述正确的是( )
如图所示,是在其他条件一定时,反应2A+B?2C△H<0,A的最大转化率与温度关系曲线,下列叙述正确的是( )| A、X或Y两点相应,V(正)>V(逆) |
| B、Z、N两点表示未达平衡状态,且都是V(正)>V(逆) |
| C、W点表示非平衡状态,V(正)>V(逆) |
| D、相应反应速率大小的点:W>Y>N |
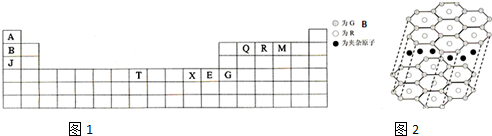
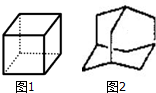 判断同分异构体的种类(不考虑立体异构):
判断同分异构体的种类(不考虑立体异构):