题目内容
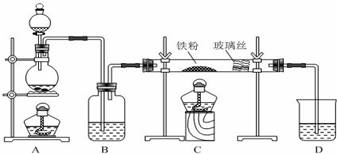
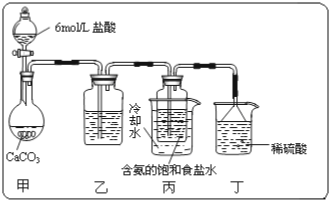
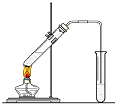
7.某活动小组进行碳酸氢钠的制备实验.有关反应的化学方程式为:NH3+CO2+H2O=NH4HCO3;NH4HCO3+NaCl=NaHCO3↓+NH4Cl(1)一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如下图所示(图中夹持、固定用的仪器未画出).试回答下列有关问题:
①实验室制氨气的化学方程式Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+CaCl2+2H2O.
②乙装置中的试剂是饱和碳酸氢钠溶液,丁装置中稀硫酸的作用是吸收未反应完的NH3.
③实验结束后,分离出NaHCO3晶体的操作是过滤(填分离操作的名称),该操作所需要的玻璃仪器有:玻璃棒和漏斗、烧杯.
(2)碳酸氢钠受热所得固体12.28g 与足量的石灰水充分反应,所得沉淀经洗涤、干燥.质量为 12.00g,则所得固体中碳酸钠的质量分数为86.3%.
分析 (1)甲装置用于制备二氧化碳,二氧化碳中混有氯化氢,则乙为饱和碳酸氢钠溶液,用于除去氯化氢,二氧化碳和氨水在丙中发生反应NH3+CO2+H2O=NH4HCO3;NH4HCO3+NaCl=NaHCO3↓+NH4Cl,生成碳酸氢钠,丁中稀硫酸用于吸收氨气,防止污染空气;
(2)碳酸氢钠分解生成碳酸钠,碳酸氢钠、碳酸钠与石灰水反应生成碳酸钙,根据碳酸钙的质量可列方程式确定碳酸钠的质量和质量分数.
解答 解:(1)①实验室用氢氧化钙和氯化铵在加热条件下反应制备氨气,反应的化学方程式为Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+CaCl2+2H2O,
故答案为:Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+CaCl2+2H2O;
②利用盐酸制取二氧化碳时,因盐酸易挥发,所以,二氧化碳中常会含有氯化氢气体,碳酸氢钠能与盐酸反应不与二氧化碳反应,所以通过碳酸氢钠的溶液是可以除掉二氧化碳气体中的氯化氢气体,实验过程中氨气可能有剩余,而稀硫酸能与氨气反应,所以稀硫酸的作用是吸收末反应的NH3,
故答案为:饱和碳酸氢钠溶液;吸收未反应完的 NH3;
③分离出NaHCO3晶体的操作是分离固体与液体,常采用的实验操作是过滤操作,常用到的仪器有玻璃棒、烧杯和漏斗,故答案为:过滤; 漏斗、烧杯;
(2)碳酸氢钠受热发生的反应为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,与足量的石灰水充分反应,
NaHCO3+Ca(OH)2=CaCO3↓+H2O+NaOH;Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;
反应生成的碳酸钙物质的量为:$\frac{12g}{100g/mol}$=0.12mol;
设加热后的固体12.28g中含碳酸钠物质的量x、碳酸氢钠物质的量为y,依据题意得到:
①x+y=0.12、②106x+84y=12.28,
根据①②解得:x=0.1mol、y=0.02mol,
则所得固体中碳酸钠的质量分数为:$\frac{0.1mol×106g/mol}{12.28g}$×100%=86.3%,
故答案为:86.3%.
点评 本题考查性质实验方案的设计,是一道有关工业制纯碱知识的一道综合实验题目,为高频考点,题目难度中等,考查学生分析和解决问题的能力,掌握制碱原理是解题的关键.

 字词句段篇系列答案
字词句段篇系列答案| A. | Al3+ | B. | Ba2+ | C. | Cl- | D. | Mg2+ |
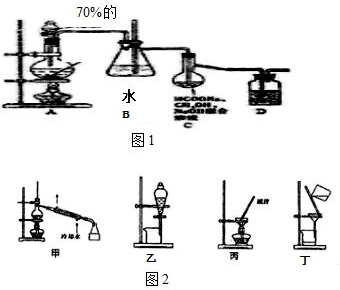
Ⅰ.某同学用乙醇、乙酸和浓硫酸制取乙酸乙酯,装置如图1所示.
(1)装置中干燥管的作用是防止小试管中液体发生倒吸
(2)小试管中的试剂加入顺序为B
A.浓硫酸 乙醇 乙酸 B.乙醇 浓硫酸 乙酸 C.乙酸 浓硫酸 乙醇
II.已知:R-OH+HX→R-X+H2O如图2是实验室用乙醇与浓硫酸和溴化钠反应制备溴乙烷的装置,图中省去了加热装置.乙醇、溴乙烷、溴有关参数数据见表:
| 乙醇 | 溴乙烷 | 溴 | |
| 状态 | 无色液体 | 无色液体 | 深红棕色液体 |
| 密度/g•cm-3 | 0.79 | 1.44 | 3.1 |
| 沸点/℃ | 78.5 | 38.4 | 59 |
(4)为除去产品中的Br2,最好选择下列溶液来洗涤产品B.
A.氢氧化钠 B.亚硫酸钠 C.碘化钠
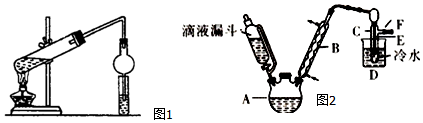
 硝基苯是医药和染料的中间体,还可做有机溶剂.反应如图:
硝基苯是医药和染料的中间体,还可做有机溶剂.反应如图:①
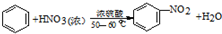
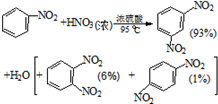
②
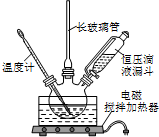
组装如图反应装置.有关数据列表如表:
| 物质 | 熔点/ ℃ | 沸点 /℃ | 密度(20℃) /g•cm-3 | 水溶性 |
| 苯 | 5.5 | 80 | 0.88 | 微溶 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶 |
| 1,3二硝基苯 | 89 | 301 | 1.57 | 微溶 |
请回答:
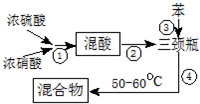
(1)步骤①配制混酸:取100mL烧杯,用20mL浓硫酸与18mL浓硝酸配制混和酸,操作是:在烧杯中先加入18mL浓硝酸,再,并不断搅拌、冷却;把配好的混和酸加入恒压漏斗中;最后在三颈烧瓶中加入18mL苯.
(2)在室温下向三颈瓶中的苯逐滴加入混酸,边滴边搅拌,混和均匀、加热.实验装置中长玻璃管最好用球形冷凝管代替(填仪器名称);上图中的加热方式称为;反应温度控制在50~60℃的原因是水浴加热、防止副反应反应.
硝基苯的提纯步骤为:

(3)步骤⑤表明混合物中有苯和硝基苯的操作和现象是混合物倒入蒸馏水中,液体分为三层.
(4)验证步骤⑥中液体已洗净的操作和现象是:取最后一次洗涤液,向溶液中加入氯化钙溶液,有白色沉淀生成,说明洗涤干净;为了得到更纯净的硝基苯,还须先向液体中加入无水CaCl2除去水,然后蒸馏(填操作名称).
(5)设计实验证明中:“粗产品中2”中含二硝基苯.
(6)用铁粉、稀盐酸与硝基苯(用Ph-NO2表示)反应可生成染料中间体苯胺(Ph-NH2),其反应的化学方程式为Ph-NO2+3Fe+6HCl→Ph-NH2+3FeCl2+2H2O.
| A. | 被氧化的元素是氯元素 | |
| B. | 氧化产物与还原产物的物质的量之比为l:1 | |
| C. | 消耗l mol还原剂,转移5 mol电子 | |
| D. | 净化1 L含CN-1.04 mg•L-1的废水,理论上需用2×l0-5mol C1O2 |
 在实验室我们用如图所示的装置制取乙酸乙酯.回答下列问题:
在实验室我们用如图所示的装置制取乙酸乙酯.回答下列问题: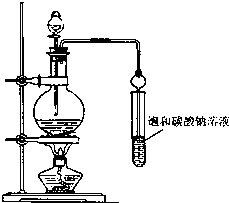 实验室合成乙酸乙酯粗产品的步骤如下:在蒸馏烧瓶内将过量的乙醇和少量浓H2SO4混合,然后经分液漏斗边滴加醋酸,边加热蒸馏,直接收集蒸馏产品可得到含有乙醇、乙醚、醋酸、少量水的乙酸乙酯粗产品.据此回答问题:
实验室合成乙酸乙酯粗产品的步骤如下:在蒸馏烧瓶内将过量的乙醇和少量浓H2SO4混合,然后经分液漏斗边滴加醋酸,边加热蒸馏,直接收集蒸馏产品可得到含有乙醇、乙醚、醋酸、少量水的乙酸乙酯粗产品.据此回答问题: CH3COOC2H5+H2O.
CH3COOC2H5+H2O.