题目内容
2.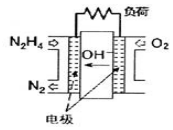 肼(N2H4)-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液.下列说法中,不正确的是( )
肼(N2H4)-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液.下列说法中,不正确的是( )| A. | 该电池放电时,通入肼的一极为负极 | |
| B. | 电池每释放1mol N2转移的电子数为4NA | |
| C. | 通入空气的一极的电极反应式是:O2+4e-+4H+=2H2O | |
| D. | 电池工作一段时间后,电解质溶液的pH将减小 |
分析 肼(N2H4)一空气燃料电池中,负极反应为:N2H4+4OH--4e-=4H2O+N2↑,正极反应为:O2+2H2O+4e-=4OH-,电池总反应为:N2H4+O2=N2↑+2H2O,结合电极方程式计算电子转移和判断溶液的pH.
解答 解:A.原电池中负极发生氧化反应,则通入的N2H4一极为负极,故A正确;
B.电池每释放1mol N2,消耗1mol的氧气,转移的电子数为4NA,故B正确;
C.通入空气的一极为正极,在碱性环境中,氧气得电子发生还原反应生成氢氧根,电极反应式为O2+2H2O+4e-=4OH-,故C错误;
D.电池总反应为N2H4+O2=N2↑+2H2O,原电池反应生成水,KOH溶液浓度降低,pH将减小,故D正确;
故选C.
点评 本题考查原电池的工作原理,注意把握电极反应式的书写,正确判断电解质溶液的pH变化,侧重于考查学生的分析能力和对基础知识的应用能力,题目难度不大.

练习册系列答案
 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案
相关题目
13.已知:pOH=-lgc(OH-),298K时,向20.00mL0.10mol•L-1氨水中滴入0.10mol•L-1的盐酸,溶液的pH和pOH与加入盐酸体积关系如图所示.下列说法正确的是( )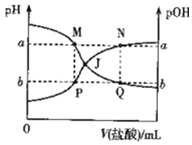

| A. | 曲线PJN表示溶液中pH的变化 | |
| B. | M点水的电离程度比Q点大 | |
| C. | M、P两点的数值之和a+b=14 | |
| D. | pH与pOH交叉点J对应的V(盐酸)=20.00 mL |
10.有机化学在日常生活应用广泛,下列有关说法不正确的是( )
| A. | 相同条件下,正丁烷、新戊烷、异戊烷的沸点依次增大 | |
| B. | 煤可与水蒸气反应制成水煤气,水煤气的主要成分为CO和H2 | |
| C. | 甲苯和Cl2光照下的反应与乙醇和乙酸反应属于同一类型的反应 | |
| D. | 苯与甲苯互为同系物,均能使KMnO4酸性溶液褪色 |
17.下列关于有机化合物的说法正确的是( )
| A. | 2,2,7,7-四甲基辛烷的一氯取代物有4种 | |
| B. | 甲醇与分子式为C3H8O的某种有机物相差2个CH2原子团,故它们一定互为同系物 | |
| C. | 苯与浓硝酸、浓硫酸共热并保持50~60℃反应生成硝基苯 | |
| D. | 甲烷和 Cl2的反应与乙烯和 Br2的反应属于同一类型的反应 |
7.下列说法正确的是( )
| A. | 干冰升华时须吸收大量的热,这就是化学反应中的吸热现象 | |
| B. | 酒精常被用作酒精灯和内燃机的燃料,说明酒精燃烧是放热反应 | |
| C. | 木炭常温下不燃烧,加热才能燃烧,说明木炭燃烧是吸热反应 | |
| D. | 酸碱中和反应都放热,因此可以将其设计成原电池,将化学能转换成电能供人们使用 |
14.汽车发动机中生成NO的反应为:N2(g)+O2(g)?2NO(g),t℃时,K=0.09.在t℃下甲、乙、丙三个恒容密闭容器中,投入N2(g) 和 O2(g) 模拟反应,起始浓度如表所示.下列判断不正确的是( )
| 起始浓度 | 甲 | 乙 | 丙 |
| c(N2)/mol•L-1 | 0.46 | 0.46 | 0.92 |
| c(O2)/mol•L-1 | 0.46 | 0.23 | 0.92 |
| A. | 起始时,反应速率:丙>甲>乙 | B. | 平衡时,c(NO):甲=丙>乙 | ||
| C. | 平衡时,N2的转化率:甲>乙 | D. | 平衡时,甲中c(N2)=0.4 mol•L-1 |
11.下列实验中,对应的实验现象以及结论都正确且两者具有因果关系的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将KI溶液滴入FeCl3溶液中,加入CCl4,振荡、静置 | 下层溶液显紫色 | 还原性:Fe2+<I- |
| B | 将SO2通入滴有酚酞的NaOH溶液中 | 溶液红色褪去 | SO2具有漂白性 |
| C | 将稀盐酸滴入Na2SiO3溶液中 | 溶液中出现凝胶 | 非金属性:Cl>Si |
| D | 将稀硫酸滴入淀粉溶液中,加热一段时间,再加入新制的Cu(OH)2悬浊液并加热 | 溶液中未出现砖红色沉淀 | 淀粉未水解 |
| A. | A | B. | B | C. | C | D. | D |
12.常温下,下列各组物质中任意两种物质均能发生反应的是( )
| 组别 物质 | 甲 | 乙 | 丙 |
| A | N2 | O2 | H2 |
| B | Al | 盐酸 | Fe2O3 |
| C | SiO2 | Cl2 | NaOH(aq) |
| D | SO2 | 氨水 | NaHCO3(aq) |
| A. | A | B. | B | C. | C | D. | D |
 .
.