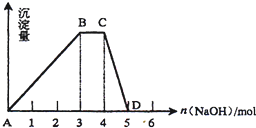
题目内容
10.由NaOH和NaHCO3组成的固体混合物33.2g,放在密闭容器中加热至300℃,经充分反应后排出气体,冷却后称得残留固体质量为26.5g,则原混合物中NaOH与NaHCO3的物质的量之比为2:3,NaOH的质量分数为24.1%% (保留小数点后一位).分析 加热发生反应:NaOH+NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O,若碳酸氢钠过量,还发生反应:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,若NaOH、NaHCO3恰好按1:1反应,固体减少质量为水的质量,根据方程式可知,生成水的质量=33.2g×$\frac{18}{124}$=4.8g,实际固体质量减少=33.2g-26.5g=6.7g>4.8g,所以碳酸氢钠过量,根据方程式计算NaHCO3的质量,进而计算NaOH的质量,再计算氢氧化钠的质量分数.
解答 解:设氢氧化钠和碳酸氢钠的物质的量分别为xmol和ymol,
NaOH+NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O,
xmol xmol xmol
若碳酸氢钠过量,还发生反应:
2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,
y-x $\frac{1}{2}$(y-x)
则:$\left\{\begin{array}{l}{40x+84y=33.2g}\\{\frac{1}{2}(y-x)+x=\frac{26.5g}{106g/mol}}\end{array}\right.$,解之得:$\left\{\begin{array}{l}{x=0.2mol}\\{y=0.3mol}\end{array}\right.$,所以混合物中NaOH与NaHCO3的物质的量之比为2:3,
NaOH的质量分数为$\frac{0.2×40}{33.2}×100%$=24.1%,故答案为:2:3;24.1%.
点评 本题考查混合物的有关计算,判断容器内发生的反应是关键,可以根据二者按物质的量之比1:1反应计算固体质量减少判断发生的反应,难度中等.

| A. | 混合前醋酸溶液中水的电离程度大 | |
| B. | 混合前c(CH3COOH)大于c(Na+) | |
| C. | 混合后若c(Na+)=c(CH3COO-),则混合前乙酸体积大 | |
| D. | 分别稀释10倍,两溶液的pH之和大于14 |
| A. | 消耗B 0.08mol | B. | x=2 | ||
| C. | A的平衡浓度是1.4mol/L | D. | 平衡时气体压强是原来的0.94倍 |
| A. | 3.2g由O2和O3组成的混合物中含有的原子数目为0.2NA | |
| B. | 高温下,0.2molFe与足量水蒸气反应,转移电子数目为0.6NA | |
| C. | 在过氧化钠与水的反应中,每消耗0.1mol过氧化钠,转移电子的数目为0.1NA | |
| D. | 在KClO3+6HCl(浓)═KCl+3Cl2↑+3H2O反应中,若产生标准状况下6.72LCl2时,转移电子数目为0.5NA |
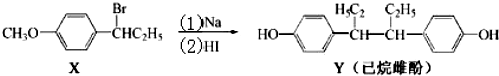
| A. | 化合物X 的分子式为C9H13BrO | B. | 化合物X苯环上的一溴代物有四种 | ||
| C. | 用FeCl3溶液可鉴别化合物X和Y | D. | 反应(2)属于取代反应 |
 已知下列数据:
已知下列数据:| 物质 | 熔点(℃) | 沸点(℃) | 密度(g•cm-3) |
| 乙醇 | -117.0 | 78.0 | 0.79 |
| 乙酸 | 16.6 | 117.9 | 1.05 |
| 乙酸乙酯 | -83.6 | 77.5 | 0.90 |
| 浓硫酸(98%) | - | 338.0 | 1.84 |
①在30mL的大试管A中按体积比1:4:4的比例配制浓硫酸、乙醇和乙酸的混合溶液;
②按图连接好装置(装置气密性良好),用小火均匀地加热装有混合溶液的大试管5~10min;
③待试管B收集到一定量的产物后停止加热,撤去试管B并用力振荡,然后静置待分层;
④分离出乙酸乙酯层、洗涤、干燥.
请根据题目要求回答下列问题:
(1)配制该混合溶液的主要操作步骤为在大试管中先加4 mL乙醇,再缓慢加入1 mL浓H2SO4,边加边振荡,待冷至室温后,再加4 mL乙酸并摇匀.
(2)上述实验中饱和碳酸钠溶液的作用是(填字母)BC.
A.中和乙酸和乙醇
B.中和乙酸并吸收部分乙醇
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出
D.加速酯的生成,提高其产率
(3)步骤②中需要小火均匀加热操作,其主要理由是防止反应物随生成物一起大量被蒸出来,导致原料损失,及发生副反应.
(4)分离出乙酸乙酯后,为了干燥乙酸乙酯可选用的干燥剂为(填字母)B.
A.P2O5 B.无水Na2SO4
C.碱石灰 D.NaOH固体
(5)浓硫酸的作用是:①催化作用;②吸水作用.
(6)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止倒吸.
(7)若要把制得的乙酸乙酯分离出来,应采用的实验操作是用饱和碳酸钠溶液承接蒸馏出的乙酸乙酯,再分液.
(8)某同学将收集到的乙酸乙酯滴入饱和NaHCO3溶液中,观察到有少量气泡产生,可得出的结论是乙酸乙酯中含有乙酸,该过程中发生反应的化学方程式是CH3COOH+NaHCO3=CH3COONa+CO2↑+H2O.
| A. | 乙烯和苯 | B. | 乙醇和丙醇(CH3CH2CH2OH) | ||
| C. | 乙醇和乙醚(C2H5OC2H5) | D. | 甲醛(HCHO)和乙酸 |
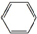 .
. ,取代反应.
,取代反应.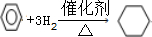 ,加成反应.
,加成反应.