题目内容
16.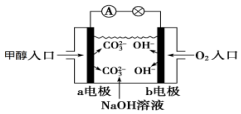 如图是甲醇燃料电池原理示意图,请回答下列问题:
如图是甲醇燃料电池原理示意图,请回答下列问题:(1)电池工作一段时间后电解质溶液的pH减小(填“增大”、“减小”或“不变”);
(2)该燃料电池的电极反应式:
正极反应式:O2+4e-+2H2O═4OH-;
负极反应式:CH3OH+8OH--6e-═CO32-+6H2O.
分析 碱性甲醇燃料电池的总反应式为2CH3OH+4OH-+3O2=2CO32-+6H2O,负极上投放燃料,发生失电子的氧化反应,正极上投放氧气,发生得电子的还原反应,据此解答.
解答 解:(1)电池的总反应式为2CH3OH+4OH-+3O2=2CO32-+6H2O,电解质溶液中的氢氧根离子被消耗,碱性减弱,pH减小,
故答案为:减小;
(2)通入氧气的b极为燃料电池的正极,发生得电子的还原反应,在碱性环境下,电极反应式为O2+4e-+2H2O═4OH-,通入甲醇的a极为燃料电池的负极,发生失电子的氧化反应,电极反应式为CH3OH+8OH--6e-═CO32-+6H2O,
故答案为:O2+4e-+2H2O═4OH-;CH3OH+8OH--6e-═CO32-+6H2O.
点评 本题考查了原电池的工作原理,涉及电极判断、电极方程式书写等相关知识,为高频考点,侧重于基础知识的考查,注意把握原电池的工作原理,题目难度不大.

练习册系列答案
相关题目
6.125℃时在容积不变的容器中:W、X、Y、Z的浓度变化如表:下列叙述中正确的是( )
| 物质 | W(g) | X(g) | Y(g) | Z(g) |
| 初始浓度(mol/L) | 4.0 | 2.0 | 0 | 0 |
| 2min末浓度(mol/L) | 2.4 | 1.2 | 0.8 | 1.6 |
| A. | 2min内X的平均速率为0.6mol/(L•min) | |
| B. | 该反应的化学方程式可表示为:2W(g)+X(g)?2Y+Z | |
| C. | 若达到平衡后保持压强不变充入Ne,平衡不移动 | |
| D. | 平衡后再加入W,则W的转化率增大 |
7.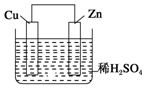 如图是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下,其中正确的是( )
如图是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下,其中正确的是( )
①Zn为正极,Cu为负极;
②H+向负极移动;
③电子是由Zn经外电路流向Cu;
④Cu极上有H2产生;
⑤若有1mol电子流过导线,则产生的H2为1g;
⑥正极的电极反应式为Zn-2e-═Zn2+.
 如图是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下,其中正确的是( )
如图是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下,其中正确的是( ) ①Zn为正极,Cu为负极;
②H+向负极移动;
③电子是由Zn经外电路流向Cu;
④Cu极上有H2产生;
⑤若有1mol电子流过导线,则产生的H2为1g;
⑥正极的电极反应式为Zn-2e-═Zn2+.
| A. | ①②③ | B. | ③④⑤ | C. | ④⑤⑥ | D. | ②③④ |
4.下列关于离子反应的说法正确的是( )
| A. | NH4HSO3与NaOH等物质的量反应:NH4++HSO3-+2OH-═NH3•H2O+SO32- | |
| B. | 铜与浓硝酸反应的离子方程式为3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O | |
| C. | 1.0 mol•L-1的KNO3溶液中可大量存在H+、Fe2+、Cl-、SO42- | |
| D. | 过量SO2通入次氯酸钠溶液:SO2+ClO-+H2O═SO42-+Cl-+2H+ |
11.发生在山东圆通的夺命快递,导致l人死亡9人中毒.从物质的角度分析,是源于氟乙酸甲酯(FCH2COOCH3)中毒引起的.下列有关氟乙酸甲酯的说法正确的是( )
| A. | 氟乙酸甲酯仅含有一种官能团 | |
| B. | 氟乙酸甲酯的同分异构体属于羧酸类的有3种 | |
| C. | lmol氟乙酸甲酯与NaOH水溶液共热最多消耗2molNaOH | |
| D. | 氟乙酸甲酯加入稀硫酸共热后生成的有机物是HOCH2COOH和CH3OH |
8.下列关系正确的是( )
| A. | 熔、沸点:戊烷>2,2一二甲基戊烷>2,3一二甲基丁烷>丙烷 | |
| B. | 密度:CH3CH2Br>H2O>甲苯 | |
| C. | 等质量的物质燃烧耗O2量:乙烯>乙炔>甲烷 | |
| D. | 等物质的量物质燃烧耗O2量:环已烷>苯>苯甲酸 |
5.下列说法正确的是( )
| A. | 在0.1mol•L-1 Ca(ClO)2溶液中K+、Na+、I-、Cl-可以大量共存 | |
| B. | 氢氧化铁溶于氢碘酸中的离子方程式为:Fe(OH)3+3H+═Fe3++3H2O | |
| C. | 等体积和等物质的量浓度的CH3COONH4和NH3•H2O混合液中c(CH3COOH)+c(CH3COO-)═c(NH4+)+c(NH3•H2O) | |
| D. | 常温下,浓度均为0.1mol•L-1的CH3COOH、CH3COONa混合溶液显酸性,则:c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+)>c(OH-) |
6.下列关于元素周期表和元素周期律的说法不正确的是( )
| A. | 第ⅦA族从氟到碘,其氢化物的稳定性逐渐减弱 | |
| B. | 同周期,从左到右,元素金属性逐渐减弱,非金属性逐渐增强(稀有气体元素除外) | |
| C. | 因为一个铝原子比一个钠原子失去电子数目多,所以铝单质比钠单质还原性强 | |
| D. | Cs是最活泼金属元素,F是最活泼非金属元素 |
 反应类型加聚反应
反应类型加聚反应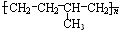 单体结构简式为CH2=CH2和CH3-CH=CH2.
单体结构简式为CH2=CH2和CH3-CH=CH2.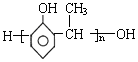 单体结构简式为
单体结构简式为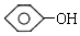 和CH3CHO.
和CH3CHO.