题目内容
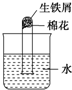 铁是用途最广的金属材料之一.为探究铁的化学性质,某同学将盛有生铁屑的试管塞上蓬松的棉花,然后倒置在水中(如图所示).数天后,他观察到的现象是( )
铁是用途最广的金属材料之一.为探究铁的化学性质,某同学将盛有生铁屑的试管塞上蓬松的棉花,然后倒置在水中(如图所示).数天后,他观察到的现象是( )| A、铁屑不生锈,试管内液面上升 |
| B、铁屑不生锈,试管内液面高度不变 |
| C、铁屑生锈,试管内液面上升 |
| D、铁屑生锈,试管内液面高度不变 |
考点:金属腐蚀的化学原理
专题:几种重要的金属及其化合物
分析:根据已有的知识进行分析,铁在有水和氧气并存时易生锈,铁生锈消耗氧气,能使试管内的压强变小.
解答:
解析:装置中的生铁屑在潮湿的空气中发生吸氧腐蚀,电池反应为2Fe+O2+2H2O→2Fe(OH)2,4Fe(OH)2+O2+2H2O→4Fe(OH)3,最终Fe(OH)3失水生成铁锈,因反应消耗氧气,使试管内气压减小,试管内液面上升,
故选C.
故选C.
点评:本题考查了金属的腐蚀原理,题目难度不大,可以依据铁生锈的条件、原理结合物理压强的知识进行.

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案
相关题目
用电解熔融氯化镁而不用电解氧化镁的方法制金属镁,可能的原因是( )
| A、易制得氯化镁,不易制得氧化镁 |
| B、溶融氧化镁不能被电解 |
| C、氧化镁熔点比氯化镁熔高得多 |
| D、氯化镁易溶于水,氧化镁不溶于水 |
除去二氧化碳中混有的少量二氧化硫气体,可选用的试剂是( )
| A、饱和食盐水 |
| B、NaOH溶液 |
| C、足量澄清石灰水 |
| D、饱和碳酸氢钠溶液 |
下列说法正确的是( )
| A、常温下,0.4mol/L HB溶液和0.2mol/L NaOH溶液等体积混合后溶液的pH=3,则混合溶液中离子浓度大小顺序为c(B-)>c(H+)>c(Na+)>c(OH-) |
| B、5mL 0.02mol/L HCl溶液与5mL 0.02mol/L Ba(OH)2溶液混合,经充分反应后,如果溶液体积为10mL,则溶液pH=12 |
| C、pH相同的①CH3COONa、②NaHCO3、③NaClO三份溶液中的c(Na+):③>②>① |
| D、0.1mol/L HA溶液与0.05mol/L NaOH溶液等体积混合后所得溶液呈酸性,则有:c(H+)+c(Na+)>c(OH-)+c(A-) |
金属钠通常保存在( )
| A、水中 | B、煤油中 |
| C、汽油中 | D、四氯化碳中 |
使用结晶方法分离混合物的依据是混合物中几种可溶性固体物质( )
| A、熔点不同 |
| B、在同一种溶剂里的溶解度不同 |
| C、沸点不同 |
| D、在不同溶剂里的溶解度不同 |
钢铁在很弱的酸性或中性条件下发生电化学腐蚀时,正极的反应式为( )
| A、Fe-2e-═Fe2+ |
| B、2H++2e-═H2↑ |
| C、2H2O+O2+4e-═4OH- |
| D、Fe-3e-═Fe3+ |