题目内容
14.a、b、c、d是HCl、BaCl2、AgNO3、Na2CO3四种溶液中的一种,现将它们两两混合,现象如表所示| 反应物 | a+b | c+d | a+d | a+c | b+d |
| 现象 | 白色沉淀 | 白色沉淀 | 白色沉淀 | 白色沉淀 | 无色气体 |
| A. | HCl、BaCl2、AgNO3、Na2CO3 | B. | AgNO3、HCl、BaCl2、Na2CO3 | ||
| C. | BaCl2、Na2CO3、AgNO3、HCl | D. | AgNO3、HCl、Na2CO3、BaCl2 |
分析 b+d反应生成无色气体,则b、d为HCl、Na2CO3中的一种,而d+c、d+a均生成白色沉淀,则d为Na2CO3,所以b为HCl,a+b反应生成白色沉淀,a为AgNO3,可知c为BaCl2,以此来解答.
解答 解:由表中反应物及现象可知,b+d反应生成无色气体,则b、d为HCl、Na2CO3中的一种,Na2CO3+2HCl═2NaCl+H2O+CO2↑,
又d+c、d+a均生成白色沉淀,则d为Na2CO3,所以b为HCl,
a+b反应生成白色沉淀,a为AgNO3,可知c为BaCl2,
a+b:AgNO3+HCl=AgCl↓+HNO3,c+d:BaCl2+Na2CO3=BaCO3↓+2NaCl,a+d:AgNO3+Na2CO3=Ag2CO3↓+NaNO3,a+c:2AgNO3+BaCl2=2AgCl↓+Ba(NO3)2,b+d:Na2CO3+2HCl═2NaCl+H2O+CO2↑,
故选B.
点评 本题考查物质的推断,明确物质的性质及发生的反应中的现象是解答本题的关键,注意把握物质的性质,b与d反应及d的推断是解答本题的突破口,题目难度不大.

练习册系列答案
相关题目
2.化学与生产、生活紧密相关,下列物质的性质和用途均正确且有因果关系的是( )
| 选项 | 性质 | 用途 |
| A | 糖类、油脂和蛋白质均能水解 | 供给人类营养 |
| B | 铁能被浓硫酸钝化 | 铁制器皿用作铜和浓硫酸的反应容器 |
| C | 碳单质的还原性强于硅单质 | 碳与石英反应冶炼粗硅 |
| D | 常温下,氨气能与氯气反应 | 浓氨水检验氯气管道泄漏 |
| A. | A | B. | B | C. | C | D. | D |
5.下列离子方程式书写正确的是( )
| A. | FeCl2溶液中通入氯气:Fe2++Cl2=Fe3++2Cl- | |
| B. | FeS固体放入稀硝酸溶液中:FeS+2H+=Fe2++H2S↑ | |
| C. | 碳酸氢镁和足量的氢氧化钙溶液反应:Ca2++OH-+HCO3-=CaCO3↓+H2O | |
| D. | 向明矾溶液中滴加Ba(OH)2溶液,恰好使Al3+沉淀完全:2Al3++3SO42-+3Ba2++6OH-=2 Al(OH)3↓+3BaSO4↓ |
9.某化学反应2A?B+D在四种不同条件下进行,B、D起始浓度为0.反应物A的浓度(mol/L)随反应时间(min)的变化情况如表:
根据上述数据,完成下列填空:
(1)在实验1,反应在10至20分钟时间内平均速率为0.013mol/(L•min).
(2)设实验3的反应速率为v3,实验1的反应速率为v1,则v3>v1(填>、=、<),且c3>1.0mol/L(填>、=、<)
(3)比较实验4和实验1,可推测该反应是吸热反应(选填吸热、放热).理由是由实验1到实验4升高温度,平衡右移,加热平衡向吸热反应方向移动.
| 实验序号 | 时间 浓度 温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | c3 | 0.92 | 0.75 | 0.60 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
(1)在实验1,反应在10至20分钟时间内平均速率为0.013mol/(L•min).
(2)设实验3的反应速率为v3,实验1的反应速率为v1,则v3>v1(填>、=、<),且c3>1.0mol/L(填>、=、<)
(3)比较实验4和实验1,可推测该反应是吸热反应(选填吸热、放热).理由是由实验1到实验4升高温度,平衡右移,加热平衡向吸热反应方向移动.
6.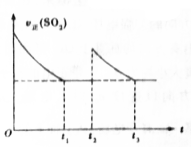 一定温度下,密闭容器中进行反应:2SO2(g)+O2(g)?2SO3(g)△H<0.测得v正(SO2)随反应时间(t)的变化如图所示.下列有关说法正确的是( )
一定温度下,密闭容器中进行反应:2SO2(g)+O2(g)?2SO3(g)△H<0.测得v正(SO2)随反应时间(t)的变化如图所示.下列有关说法正确的是( )
 一定温度下,密闭容器中进行反应:2SO2(g)+O2(g)?2SO3(g)△H<0.测得v正(SO2)随反应时间(t)的变化如图所示.下列有关说法正确的是( )
一定温度下,密闭容器中进行反应:2SO2(g)+O2(g)?2SO3(g)△H<0.测得v正(SO2)随反应时间(t)的变化如图所示.下列有关说法正确的是( )| A. | t2时改变的条件是:只加入一定量的SO2 | |
| B. | t1时平衡常数K1大于t3时平衡常数K2 | |
| C. | t1时平衡混合气的$\overline{{M}_{1}}$大于t3时平衡混合气的$\overline{{M}_{2}}$ | |
| D. | t1时平衡混合气中的SO3的体积分数等于t3时平衡混合气中SO3的体积分数 |
6.下列物质中不能用化合反应的方法制得的是( )
①SiO2 ②H2SiO3 ③Fe(OH)3 ④CuS ⑤FeCl2 ⑥CaSiO3.
①SiO2 ②H2SiO3 ③Fe(OH)3 ④CuS ⑤FeCl2 ⑥CaSiO3.
| A. | ②④ | B. | ②④⑤ | C. | ②③④⑤ | D. | ②④⑥ |

