题目内容
16.25°C时,pH=2的某酸HnA(An-为酸根)与pH=12的某碱B(OH)m等体积混合,混合液的pH变为5.下列判断正确的是( )| A. | 生成的正盐化学式为BmAn | |
| B. | 该盐中存在着一定水解的离子,该离子水解方程式为:Bm++mH2O?B(OH)m+mH+ | |
| C. | 生成的盐为强酸弱碱盐 | |
| D. | HnA为弱酸,其第一步电离方程式为:HmA?Hm-1A-+H+ |
分析 常温下PH=2的某酸HnA(A为酸根)与PH=12的某碱B(OH)m等体积混合,混合液的PH变为5,说明HnA为弱酸,且酸过量,根据化合物中化合价的代数和为0确定其化学式,根据酸碱的相对强弱确定水解的离子.
解答 解:A、HnA中A的化合价是-n价,B(OH)m中B的化合价是+m价,根据化合物中化合价的代数和为0知,二者的离子个数之比为n:m,则其化学式为:BnAm,
故A错误;
B、根据题意知,HnA为弱酸,则An-离子一定能水解,其水解方程式为:An-+H2O?HA(n-1)-+OH-,故B错误;
C、HnA为弱酸,生成的盐为弱酸强碱盐,故C错误;
D、HnA为弱酸,分步电离,其第一步电离方程式为:HmA?Hm-1A-+H+,故D正确.
故选D.
点评 本题考查了酸碱混合溶液定性判断,明确“谁强谁显性、谁弱谁水解”即可解答,并结合化合物中化合价的代数和为0进行分析,难度中等.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案 小学学习好帮手系列答案
小学学习好帮手系列答案
相关题目
3.将NO2与氧气以一定比例通入足量水中,得到溶液,关于这份溶液,下列说法正确的是( )
| A. | 若NO2与O2的体积比是4:3,则此溶液除了硝酸不含其他杂质 | |
| B. | 将一定量的Cu投入溶液中,只产生1.12L(标况)的红棕色气体,则反应的铜有1.6g | |
| C. | 将溶液在强光下光照,产生气泡,溶液变浅黄,产生气泡,则气泡是NO2 | |
| D. | 向浅黄的硝酸中通入氧气,可以使其pH值降低,溶液质量不变 |
4.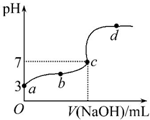 已知在25℃条件下向10.00mL 0.1mol•L-1HCOOH溶液中逐滴加入0.1mol•L-1NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中不正确的是( )
已知在25℃条件下向10.00mL 0.1mol•L-1HCOOH溶液中逐滴加入0.1mol•L-1NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中不正确的是( )
 已知在25℃条件下向10.00mL 0.1mol•L-1HCOOH溶液中逐滴加入0.1mol•L-1NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中不正确的是( )
已知在25℃条件下向10.00mL 0.1mol•L-1HCOOH溶液中逐滴加入0.1mol•L-1NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中不正确的是( )| A. | a点表示的溶液中c(HCOO-)约为10-3mol•L-1 | |
| B. | 用25 mL的酸式滴定管量取HCOOH溶液 | |
| C. | c点NaOH溶液的体积小于10 mL | |
| D. | 在a、c间任一点,溶液中一定都有c(HCOO-)>c(Na+)>c(H+)>c(OH-) |
11.25℃时,向a mL 2.0mol•L-1的NaOH溶液中加入2.0mol•L-1的醋酸溶液,当加入bmL醋酸溶液时,混合溶液的pH为7,假设混合溶液的体积为(a+b)mL,已知,醋酸的电离平衡常数1.75×10-5,则$\frac{a}{b}$的值为( )
| A. | $\frac{175}{176}$ | B. | $\frac{100}{99}$ | C. | $\frac{99}{100}$ | D. | $\frac{1}{2}$ |
1.下列说法正确的是( )
| A. | 改变条件,反应物的转化率增大,平衡常数也一定增大 | |
| B. | 常温下,V1L pH=12的NaOH溶液与V2L pH=2的HA溶液混合,若混合液显中性,则V1≤V2 | |
| C. | 在0.1mol•L-1 NaHCO3溶液中,加入少量NaOH固体,Na+和CO32-的离子浓度均增大 | |
| D. | 原子晶体与分子晶体在溶于水和熔化时化学键均断裂 |
5.一定条件下,氨气和氟气发生反应:4NH3+3F2→NF3+3NH4F,其中产物NF3分子结构和NH3相似.下列有关说法错误的是( )
| A. | NF3分子呈三角锥形 | |
| B. | NF3分子是极性分子 | |
| C. | NF3与NH3晶体类型相同 | |
| D. | 上述反应的反应物和生成物均属于共价分子 |
6.在氨水中存在NH3•H2O?NH4++OH-的平衡,若要使平衡向逆方向移动,同时使c(OH-)增大,应加入( )
| A. | 氯化铵固体 | B. | 硫酸 | C. | NaOH固体 | D. | 大量水 |

 常温下有0.1mol•L-1五种溶液NaOH、NH3•H2O、CH3COOH、HCl、NH4HSO4.
常温下有0.1mol•L-1五种溶液NaOH、NH3•H2O、CH3COOH、HCl、NH4HSO4.