题目内容
5.只用一种试剂就能将甲苯、环己烯、四氯化碳、碘化钾溶液区分开来,该试剂可以是( )| A. | 溴化钾溶液 | B. | 溴水 | C. | 高锰酸钾溶液 | D. | 硝酸银溶液 |
分析 甲苯和四氯化碳都比溶于水,且二者的密度不同,烯烃含有碳碳双键,可发生加成、氧化反应,碘化钾溶于水,具有还原性,根据物质的性质的异同选择合适的鉴别试剂.
解答 解:A.溴化钾溶液与四种试剂都不反应,溴化钾溶液与碘化钾溶液互溶,甲苯、环己烯、四氯化碳都不溶于水,溶液分层,四氯化碳密度比水大,有机层在下层,而甲苯、己烯且密度都比水小,有机层在生成,不能鉴别,故A错误;
B.甲苯不溶于水,但密度比水小,四氯化碳不溶于水,但密度比水大,加入溴水,色层位置不同,环己烯与溴水发生加成反应,碘化钾与溴水发生氧化还原反应,溶液颜色加深,可鉴别,故B正确;
C.甲苯、环己烯、碘化钾溶液与酸性高锰酸钾发生氧化还原反应,均使酸性高锰酸钾溶液褪色,不能鉴别,故C错误;
D.加入硝酸银溶液,不能鉴别甲苯和环己烯,二者与硝酸银不反应,且密度都比水小不能鉴别,故D错误.
故选B.
点评 本题考查有机物的鉴别,为高频考点,把握有机物的结构与性质、有机反应及现象为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
15.根据同分异构体的概念,判断下列物质互为同分异构体的是( )
| A. | CH3-CH2-NO2 和 H2N-CH2-COOH | B. | H和D | ||
| C. | 甲烷和正丁烷 | D. | 红磷和白磷 |
16.按要求回答下列问题.
(1)A元素的负一价离子的电子层结构与氩相同,它在元素周期表中的位置为第三周期第VIIA族
(2)B元素基态原子的最外层有2个未成对电子,次外层有2个电子,其元素名称为碳或氧
(3)D元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,D的最外层电子排布式
为4s1
(4)X元素的原子最外层电子排布式为nsnnpn+1,Y元素的某同位素原子无中子.X和Y形成的最简单化合物的结构式为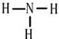
(5)M元素的正三价离子的3d能级为半充满,M基态原子的电子排布式为1s22s22p63s23p63d64s2
(6)如表是N逐级失去电子的电离能.
则元素N的常见价态是+3价.
(1)A元素的负一价离子的电子层结构与氩相同,它在元素周期表中的位置为第三周期第VIIA族
(2)B元素基态原子的最外层有2个未成对电子,次外层有2个电子,其元素名称为碳或氧
(3)D元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,D的最外层电子排布式
为4s1
(4)X元素的原子最外层电子排布式为nsnnpn+1,Y元素的某同位素原子无中子.X和Y形成的最简单化合物的结构式为
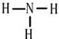
(5)M元素的正三价离子的3d能级为半充满,M基态原子的电子排布式为1s22s22p63s23p63d64s2
(6)如表是N逐级失去电子的电离能.
| I1 | I2 | I3 | I4 | I5 | I6 | |
| In | 578 | 1817 | 2745 | 11578 | 14831 | 18378 |
13.下列说法错误的是( )
| A. | 化学键的断裂和形成是化学反应中能量变化的主要原因 | |
| B. | 煤炭燃烧前经过脱硫处理可减少酸雨的产生 | |
| C. | 燃料电池是一种高效、友好的发电装置,可将化学能完全转化为电能 | |
| D. | 太阳能的利用,一般是将太阳辐射能先转化为热能、电能或化学能,再加以利用 |
20.下列指定溶液中一定能大量共存的离子组是( )
| A. | pH=1的溶液中:NH4+、Na+、Fe3+、SO42- | |
| B. | 含有大量AlO2-的溶液中:Na+、K+、HCO3-、NO3- | |
| C. | 中性溶液中:K+、Fe3+、Cl-、SO42- | |
| D. | Na2S溶液中:SO42-、K+、Cu2+、Cl- |
10.X、Y、Z、W是元素周期表前四周期中常见的元素,原子序数依次增大.其相关信息如下表:
(1)X的电负性比Y的小(填“大”或“小”);X 和Y的气态氢化物中,较稳定的是H2O(写化学式).
(2)W在周期表中的位置是第四周期第Ⅷ族,其基态原子价电子的电子排布式为3d64s2.
(3)Z2Y2的电子式为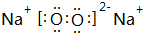 ,请写出Z2Y2与XY2反应的化学方程式2Na2O2+2CO2=2Na2CO3+O2.
,请写出Z2Y2与XY2反应的化学方程式2Na2O2+2CO2=2Na2CO3+O2.
(4)在XY2分子中X原子的杂化方式为sp,其分子的空间构型为直线形.氢、X、Y三种元素可共同形成多种分子和一种常见无机阴离子,写出其中一种分子与该无机阴离子反应的离子方程式:HCO3-+CH3COOH=CH3COO-+CO2↑+H2O.
| 元素 | 相关信息 |
| X | X的基态原子价层电子中有两个未成对电子 |
| Y | Y的基态原子最外层电子排布式为:nsnnpn+2 |
| Z | Z存在质量数为23,中子数为12的核素 |
| W | W有多种化合价,其白色氢氧化物在空气中会迅速变成灰绿色,最后变成红褐色 |
(2)W在周期表中的位置是第四周期第Ⅷ族,其基态原子价电子的电子排布式为3d64s2.
(3)Z2Y2的电子式为
 ,请写出Z2Y2与XY2反应的化学方程式2Na2O2+2CO2=2Na2CO3+O2.
,请写出Z2Y2与XY2反应的化学方程式2Na2O2+2CO2=2Na2CO3+O2.(4)在XY2分子中X原子的杂化方式为sp,其分子的空间构型为直线形.氢、X、Y三种元素可共同形成多种分子和一种常见无机阴离子,写出其中一种分子与该无机阴离子反应的离子方程式:HCO3-+CH3COOH=CH3COO-+CO2↑+H2O.
17.已知:(1)2H2(g)+O2(g)═2H2O(g);△H=a kJ•mol-1
(2)H2(g)+$\frac{1}{2}$O2(g)═H2O(g);△H=b kJ•mol-1
(3)2H2(g)+O2(g)═2H2O(l);△H=c kJ•mol-1
(4)H2(g)+$\frac{1}{2}$O2(g)═H2O(l);△H=d kJ•mol-1
下列关系式中,正确的是( )
(2)H2(g)+$\frac{1}{2}$O2(g)═H2O(g);△H=b kJ•mol-1
(3)2H2(g)+O2(g)═2H2O(l);△H=c kJ•mol-1
(4)H2(g)+$\frac{1}{2}$O2(g)═H2O(l);△H=d kJ•mol-1
下列关系式中,正确的是( )
| A. | a=2b<0 | B. | a=2c<0 | C. | c=2d>0 | D. | c>a>b |
14.把m mol乙烯跟n mol H2混合于一密闭容器中,在适当条件下反应并生成p molC2H6,若将所得混合气体燃烧,并全部生成CO2和H2O,需要氧气的物质的量为( )
| A. | 3m+n | B. | 3m+$\frac{n}{2}$ | C. | 3m+3p+$\frac{n}{2}$ | D. | 3m+$\frac{n}{2}$-3p |
15.下列离子的检验方法中正确的是( )
| A. | 某溶液加AgNO3溶液生成白色沉淀,说明原溶液中有Cl- | |
| B. | 某溶液加BaCl2溶液生成白色沉淀,说明原溶液中有SO42- | |
| C. | 某溶液加NaOH溶液生成蓝色沉淀,说明原溶液中有Mg2+ | |
| D. | 某溶液加NaOH溶液生成红褐色沉淀,说明原溶液中有Fe3+ |