题目内容
雾霾天气严重影响了人们的生活质量,其中氮氧化物和硫氧化物是造成雾霾天气的主要原因之一.
Ⅰ.将PM2.5样本用蒸馏水处理制成待测试样.
若测得该样本所含水溶性无机离子的化学组分及其浓度如下表:
根据表中数据判断该试样的pH=
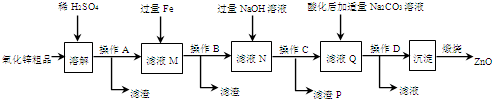
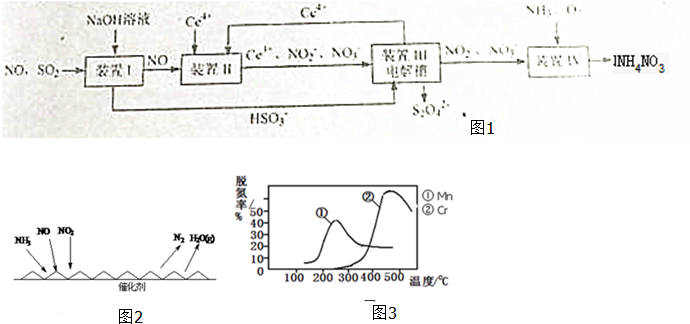
(1)方法一:工业上变“废”为宝,吸收工业尾气SO2和NO,可获得Na2S2O4(连二亚硫酸钠)和NH4NO3 产品的流程图如图1(Ce为铈元素):
①装置Ⅰ中的主要反应的离子方程式为 ;
②装置Ⅲ可以使Ce4+中再生,若用甲烷燃烧电池电解该装置中的溶液,当消耗1mol甲烷时,理论上可再生 molCe4+.
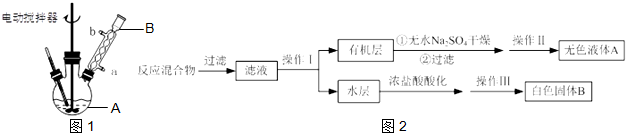
方法二:NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术.反应原理如图2所示:
①图3是不同催化剂Mn和Cr在不同温度下对应的脱氢率,由图综合考虑可知最佳的催化剂和相应的温度分别为 (填序号)
a.Mn,200℃左右、b.Cr,450℃左右、c.Mn和Cr,300℃左右.
②用Fe做催化剂时,在氨气足量的情况下,不同
=1:1脱氢效果最佳.已知生成11.2L N2(标)反应放出的热量为QkJ,此时对应的脱氢反应的热化学方程式为 .
Ⅰ.将PM2.5样本用蒸馏水处理制成待测试样.
若测得该样本所含水溶性无机离子的化学组分及其浓度如下表:
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol?L-1 | 3×10-6 | 7×10-6 | 2×10-5 | 3×10-5 | 5×10-5 | 2×10-5 |
(1)方法一:工业上变“废”为宝,吸收工业尾气SO2和NO,可获得Na2S2O4(连二亚硫酸钠)和NH4NO3 产品的流程图如图1(Ce为铈元素):
①装置Ⅰ中的主要反应的离子方程式为
②装置Ⅲ可以使Ce4+中再生,若用甲烷燃烧电池电解该装置中的溶液,当消耗1mol甲烷时,理论上可再生
方法二:NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术.反应原理如图2所示:
①图3是不同催化剂Mn和Cr在不同温度下对应的脱氢率,由图综合考虑可知最佳的催化剂和相应的温度分别为
a.Mn,200℃左右、b.Cr,450℃左右、c.Mn和Cr,300℃左右.
②用Fe做催化剂时,在氨气足量的情况下,不同
| c(NO2) |
| c(NO) |

考点:pH的简单计算,制备实验方案的设计
专题:
分析:Ⅰ、依据电荷守恒,计算溶液中含有的是氢离子还是氢氧根,然后计算pH值即可;
Ⅱ、(1)①二氧化硫是酸性氧化物,能和强碱之间发生反应;
②1molCe3+再生转化为Ce4+,提供电子为1mol,1mol甲烷完全燃烧,转移电子为mol,据此解答即可;
(2)①温度越高,对设备的要求越高,所以如果催化剂在较低温度下能较大程度的脱氢即可;根据纵坐标判断,相同温度下,脱氢率越高的效果越好;生成1mol氮气放出QkJ热量,则生成2mol氮气放出2QkJ热量.
Ⅱ、(1)①二氧化硫是酸性氧化物,能和强碱之间发生反应;
②1molCe3+再生转化为Ce4+,提供电子为1mol,1mol甲烷完全燃烧,转移电子为mol,据此解答即可;
(2)①温度越高,对设备的要求越高,所以如果催化剂在较低温度下能较大程度的脱氢即可;根据纵坐标判断,相同温度下,脱氢率越高的效果越好;生成1mol氮气放出QkJ热量,则生成2mol氮气放出2QkJ热量.
解答:
解:Ⅰ、溶液中遵循电荷守恒:c(K+)+c(NH4+)+c(Na+)+c(H+)=2c(SO42-)+c(NO3-)+c(Cl-)+c(OH-)和KW,即:3×10-6+7×10-6+3×10-5+c(H+)=2×3×10-5+5×10-5+2×10-5,解c(H+)=10-4mol?L-1,pH值为4,故答案为:4;
Ⅱ、(1)①二氧化硫是酸性氧化物,能和强碱氢氧化钠之间发生反应:SO2+OH-=HSO3-,NO和氢氧化钠之间不会反应,故答案为:SO2+OH-=HSO3-;
②甲烷燃料电池中,在碱性溶液中,甲烷燃料电池的负极反应式为CH4-8e-+10OH-═CO32-+7H2O,故每有1mol甲烷反应,转移电子数为8mol,每生成1molCe4+,提供电子为1mol,故答案为:8;
(2)①根据图象知,脱氢率越高越好,但Cr作催化剂时温度高于Mn,温度越高,对设备要求越高,增大生产成本,且脱氢率增大较小,所以使用Mn作催化剂较好;根据图象知,在温度为200-250℃或范围内间任意温度,脱氢率较高,故答案为:a;
②生成0.5mol氮气放出QkJ热量,则生成2mol氮气放出4QkJ热量,则其热化学反应方程式为2NH3(g)+NO(g)+NO2(g)?2N2(g)+3H2O(g)△H=-4QkJ/mol,
故答案为:2NH3(g)+NO(g)+NO2(g)?2N2(g)+3H2O(g)△H=-4QkJ/mol.
Ⅱ、(1)①二氧化硫是酸性氧化物,能和强碱氢氧化钠之间发生反应:SO2+OH-=HSO3-,NO和氢氧化钠之间不会反应,故答案为:SO2+OH-=HSO3-;
②甲烷燃料电池中,在碱性溶液中,甲烷燃料电池的负极反应式为CH4-8e-+10OH-═CO32-+7H2O,故每有1mol甲烷反应,转移电子数为8mol,每生成1molCe4+,提供电子为1mol,故答案为:8;
(2)①根据图象知,脱氢率越高越好,但Cr作催化剂时温度高于Mn,温度越高,对设备要求越高,增大生产成本,且脱氢率增大较小,所以使用Mn作催化剂较好;根据图象知,在温度为200-250℃或范围内间任意温度,脱氢率较高,故答案为:a;
②生成0.5mol氮气放出QkJ热量,则生成2mol氮气放出4QkJ热量,则其热化学反应方程式为2NH3(g)+NO(g)+NO2(g)?2N2(g)+3H2O(g)△H=-4QkJ/mol,
故答案为:2NH3(g)+NO(g)+NO2(g)?2N2(g)+3H2O(g)△H=-4QkJ/mol.
点评:本题主要考查的是图象分析,涉及热化学反应方程式书写,pH计算、氧化还原反应反应等,综合性较强,难度较大.

练习册系列答案
相关题目
迷迭香酸具有抗氧化、延缓衰老、减肥降脂等功效,它的结构简式为:
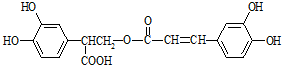 ,以邻苯二酚为原料合成迷迭香酸的路线为:
,以邻苯二酚为原料合成迷迭香酸的路线为:
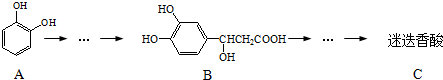
下列说法正确的是( )
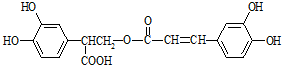 ,以邻苯二酚为原料合成迷迭香酸的路线为:
,以邻苯二酚为原料合成迷迭香酸的路线为:
下列说法正确的是( )
| A、有机物A分子中所有原子一定在同一平面上 |
| B、有机物C在浓硫酸催化下水解的一种产物是B |
| C、有机物B可以发生取代、加成、消去、氧化反应 |
| D、1 mol迷迭香酸分别与足量的NaOH溶液、浓溴水反应,最多可消耗NaOH、Br2均为6 mol |
下列离子方程式书写正确的是( )
| A、氯气通入碘化钾溶液:Cl2+I-=Cl-+I2 |
| B、稀盐酸与氨水混合:H++OH-=H2O |
| C、碳酸钠溶液与稀盐酸混合:CO32-+2H+=H2O+CO2↑ |
| D、稀硫酸滴在铜片上:Cu+2H+=Cu2++H2↑ |
下列说法正确的是( )
| A、乙烯和聚乙烯都能使溴的四氯化碳溶液褪色 |
| B、蔗糖是高分子化合物,其水解产物能发生银镜反应 |
| C、淀粉和纤维素都可以作为工业上生产葡萄糖的原料 |
| D、蛋白质溶液中加入BaCl2溶液析出沉淀,此过程叫盐析 |