题目内容
7.按要求写出下列反应的离子方程式.(1)硫酸与氢氧化钡溶液2H++2OH-+Ba2++SO42-═BaSO4↓+2H2O;
(2)碳酸钙溶于硝酸CaCO3+2H+═Ca2++CO2↑+H2O;
(3)硝酸银与氯化钠溶液Ag++Cl-═AgCl↓;
(4)铁与硫酸铜Fe+Cu2+═Fe2++Cu.
分析 (1)反应生成硫酸钡和水;
(2)反应生成硝酸钙、水、二氧化碳;
(3)反应生成AgCl和硝酸钠;
(4)反应生成硫酸亚铁和Cu.
解答 解:(1)反应生成硫酸钡和水,离子反应为2H++2OH-+Ba2++SO42-═BaSO4↓+2H2O,故答案为:2H++2OH-+Ba2++SO42-═BaSO4↓+2H2O;
(2)反应生成硝酸钙、水、二氧化碳,离子反应为CaCO3+2H+═Ca2++CO2↑+H2O,故答案为:CaCO3+2H+═Ca2++CO2↑+H2O;
(3)反应生成AgCl和硝酸钠,离子反应为Ag++Cl-═AgCl↓,故答案为:Ag++Cl-═AgCl↓;
(4)反应生成硫酸亚铁和Cu,离子反应为Fe+Cu2+═Fe2++Cu,故答案为:Fe+Cu2+═Fe2++Cu.
点评 本题考查离子反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、置换反应的离子反应及分析与应用能力的考查,注意离子反应中保留化学式的物质及电荷守恒,题目难度不大.

练习册系列答案
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案
相关题目
17.下列物质中属于非电解质的是( )
①液态HCl②熔融NaCl③蔗糖④氯水⑤Al2O3 ⑥Al(OH)3⑦Cu⑧CaCO3⑨SO2⑩乙醇.
①液态HCl②熔融NaCl③蔗糖④氯水⑤Al2O3 ⑥Al(OH)3⑦Cu⑧CaCO3⑨SO2⑩乙醇.
| A. | ③⑤⑨ | B. | ①③⑨ | C. | ③⑨⑩ | D. | ③⑦⑨ |
18.短周期主族元素X、Y、W、Z、R的原子序数依次增大.其中X、Z同主族,Z的单质是一种良好的半导体材料,W3+与Y2-具有相同的核外电子数,R是同周期中原子半径最小的元素.下列叙述正确的是( )
| A. | Y、Z形成的化合物为离子化合物 | |
| B. | Y2-的离子半径大于W3+的离子半径 | |
| C. | W的最高价氧化物对应的水化物的酸性比X的强 | |
| D. | Z的气态简单氢化物的稳定性比R的强 |
15.下列离子检验的推理正确的是( )
| A. | 向某溶液中加盐酸,有能使澄清石灰水变浑浊的气体生成,则原溶液中有CO32- | |
| B. | 向某溶液中加石蕊试液,溶液变红,则原溶液中溶质是酸 | |
| C. | 向某溶液中加氢氧化钠溶液,生成蓝色沉淀,则原溶液中有Cu2+ | |
| D. | 向某溶液中加氯化钡溶液,生成白色沉淀,再加盐酸沉淀不溶解,则原溶液中有SO42- |
2.1918年,Lewis提出反应速率的碰撞理论:反应物分子间的相互碰撞是反应进行的必要条件,但并不是每次碰撞都能引起反应,只有少数碰撞能发生化学反应.能引发化学反应的碰撞称之为有效碰撞.
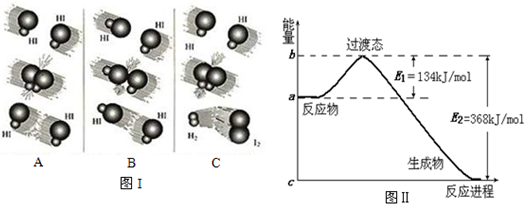
(1)图Ⅰ是HI分解反应中HI分子之间的几种碰撞示意图,其中属于有效碰撞的是C(选填“A”、“B”或“C”);
(2)图Ⅱ是1mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,则写出该反应的热化学方程式NO2(g)+CO(g)=CO2(g)+NO(g)△H=-234 kJ/mol
(3)E1的大小对该反应的反应热有无影响?无.(选填“有”或“无”)
(4)进一步研究表明,化学反应的能量变化(△H)与反应物和生成物的键能有关.键能可以简单的理解为断开1mol化学键时所需吸收的能量.如表是部分化学键的键能数据:
已知:反应CH4(g)+Cl2(g)═CH3Cl(g)+HCl(g);△H=-106kJ/mol,则表中X=413.
(5)已知:①C(s)+O2(g)═CO2(g);△H=-393.5kJ•mol-1
②2CO(g)+O2(g)═2CO2(g);△H=-566kJ•mol-1
③TiO2(s)+2Cl2(g)═TiCl4(s)+O2(g);△H=+141kJ•mol-1
则TiO2(s)+2Cl2(g)+2C(s)═TiCl4(s)+2CO(g)的△H=-80KJ/mol.

(1)图Ⅰ是HI分解反应中HI分子之间的几种碰撞示意图,其中属于有效碰撞的是C(选填“A”、“B”或“C”);
(2)图Ⅱ是1mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,则写出该反应的热化学方程式NO2(g)+CO(g)=CO2(g)+NO(g)△H=-234 kJ/mol
(3)E1的大小对该反应的反应热有无影响?无.(选填“有”或“无”)
(4)进一步研究表明,化学反应的能量变化(△H)与反应物和生成物的键能有关.键能可以简单的理解为断开1mol化学键时所需吸收的能量.如表是部分化学键的键能数据:
| 化学键 | C-H | Cl-Cl | C-Cl | H-Cl |
| 键能/kJ•mol-1 | X | 243 | 330 | 432 |
(5)已知:①C(s)+O2(g)═CO2(g);△H=-393.5kJ•mol-1
②2CO(g)+O2(g)═2CO2(g);△H=-566kJ•mol-1
③TiO2(s)+2Cl2(g)═TiCl4(s)+O2(g);△H=+141kJ•mol-1
则TiO2(s)+2Cl2(g)+2C(s)═TiCl4(s)+2CO(g)的△H=-80KJ/mol.
12.13.2g硫酸铵样品,可能混有下列物质.将该样品在加热条件下与过量氢氧化钠溶液反应,可收集到4.3L(标准状况下)气体,则该样品中不可能含有的物质是( )
| A. | 碳酸氢铵和硝酸铵 | B. | 碳酸铵和硝酸铵 | ||
| C. | 碳酸氢铵和氯化铵 | D. | 碳酸铵和氯化铵 |
19.在一定条件下,能使A(g)+B(g)?C(g)+D(g)正反应速率增大的措施是( )
| A. | 减小C和D的浓度 | B. | 增大D的浓度 | C. | 减小B的浓度 | D. | 增大A和B的浓度 |
16.已知化学反应2C(s)+O2(g)$\frac{\underline{\;点燃\;}}{\;}$ 2CO(g),2CO(g)+O2(g)$\frac{\underline{\;点燃\;}}{\;}$ 2CO2(g)都是放热反应.据此判断,下列说法中不正确的是( )
| A. | 12g C和32g O2所具有的总能量大于44g CO2所具有的总能量 | |
| B. | 12g C所具有的能量一定高于28g CO所具有的能量 | |
| C. | 56g CO和32g O2所具有的总能量大于88gCO2所具有的总能量 | |
| D. | 将一定质量的C燃烧,生成CO2比生成CO时放出的热量多 |