题目内容
3.下列有关叙述正确的是( )| A. | “歼-20”飞机上大量使用的碳纤维是一种新型的有机高分子材料 | |
| B. | 铝合金的大量使用是因为人们能用氢气等还原剂从氧化铝中获取铝 | |
| C. | 酸碱指示剂变色、煤的液化、海水提溴、皂化反应都涉及化学变化 | |
| D. | 金属镁着火可使用干粉灭火器灭火,但不可用泡沫灭火器灭火 |
分析 A.碳纤维为碳的单质,属于无机物;
B.铝的冶炼采用电解法,是电解熔融的氧化铝;
C.有新物质生成的是化学变化;
D.干粉的主要成分是碳酸氢钠(NaHCO3),受热后生成纯碱、水和二氧化碳,镁能在二氧化碳中燃烧.
解答 解:A.碳纤维为碳的单质,属于无机物,所以歼-20飞机上使用的碳纤维是一种无机非金属材料,故A错误;
B.铝性质活泼,铝的冶炼不能用热还原法,应采用电解熔融的氧化铝的方法冶炼铝,故B错误;
C.酸碱指示剂变色、煤的液化、海水提溴、皂化反应都有新物质的生成,都是化学变化,故C正确;
D.干粉的主要成分是碳酸氢钠(NaHCO3),受热后生成纯碱、水和二氧化碳,镁能在二氧化碳中燃烧,反应方程式为2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C,且生成的碳能燃烧,所以不能用干粉灭火器灭火,故D错误;
故选C.
点评 本题为综合题,涉及常见的材料及性能、金属的冶炼、物理性质与化学性质,掌握基础是解题关键,题目难度不大,注意对相关知识的积累.

练习册系列答案
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
13.某同学为了探究KMnO4溶液和Na2C2O4(草酸钠)溶液的反应过程,进行如下实验:
①配制100mL 0.0400mol•L-1的Na2C2O4溶液,除用到托盘天平、药匙、烧杯、量筒、玻璃棒等仪器外,还必须用到的玻璃仪器是100 mL容量瓶、胶头滴管.
②将KMnO4溶液逐滴滴入一定体积的酸性Na2C2O4溶液中(温度相同,并不断振荡),记录的现象如下:
请分析KMnO4溶液褪色时间变化的可能原因反应生成的Mn2+对该反应有催化作用,且c(Mn2+)越大,催化效果越好.
③用配制好的0.040 0mol•L-1的Na2C2O4溶液来标定某KMnO4溶液的浓度.每次准确量取25.00mLNa2C2O4溶液,然后用酸化后的KMnO4溶液滴定.滴定三次分别消耗的KMnO4溶液的体积是20.00mL、19.80mL、20.20mL,则KMnO4溶液的浓度为0.02mol•L-1.
①配制100mL 0.0400mol•L-1的Na2C2O4溶液,除用到托盘天平、药匙、烧杯、量筒、玻璃棒等仪器外,还必须用到的玻璃仪器是100 mL容量瓶、胶头滴管.
②将KMnO4溶液逐滴滴入一定体积的酸性Na2C2O4溶液中(温度相同,并不断振荡),记录的现象如下:
| 滴入KMnO4溶液的次序 | KMnO4溶液紫色褪去所需的时间 |
| 先滴入第1滴 | 60s |
| 褪色后,再滴入第2滴 | 15s |
| 褪色后,再滴入第3滴 | 3s |
| 褪色后,再滴入第4滴 | 1s |
③用配制好的0.040 0mol•L-1的Na2C2O4溶液来标定某KMnO4溶液的浓度.每次准确量取25.00mLNa2C2O4溶液,然后用酸化后的KMnO4溶液滴定.滴定三次分别消耗的KMnO4溶液的体积是20.00mL、19.80mL、20.20mL,则KMnO4溶液的浓度为0.02mol•L-1.
14.NA代表阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 46g乙醇中存在的共价键总数为7NA | |
| B. | 1 mol-OH和1 molOH-所含电子数均为9NA | |
| C. | 密闭容器中1molNO与1molO2充分反应,产物的原子数为4NA | |
| D. | 标准状况下,22.4L庚烷完全燃烧生成二氧化碳分子数为8NA |
18.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 0.1 mol NaOH中含有的阴离子数目为0.1NA | |
| B. | 1 L0.05mol?L-1 CH3 COOH溶液中含有的H+数目为0.05NA | |
| C. | 标准状况下,44.8 LCCl4含有的分子数为2NA | |
| D. | 反应:ClO3-+5Cl-+6H+=3Cl2+3H2O中,每生成1mol Cl2,转移的电子数为2NA |
13.下列实验操作与实验目的或结论一致的是( )
| 选项 | 实验操作 | 实验目的或结论 |
| A | 将0.1mol•L-1 Na2CO3溶液滴入BaCl2溶液至不再有沉淀产生,再滴加0.1mol•L-1 Na2SO4溶液,无明显现象 | 证明Ksp(BaSO4)> Ksp(BaCO3) |
| B | 向盛有KI3溶液的两试管中分别加入淀粉溶液和AgNO3溶液,前者溶液变蓝色,后者有黄色沉淀 | 证明KI3溶液中存在I3-?I2+I-平衡 |
| C | 向NaAlO2溶液中持续通入气体Y,先出现白色沉淀,最终沉淀又溶解 | Y可能是CO2气体 |
| D | 用硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中,溶液变黄色 | 证明氧化性:H2O2比Fe3+强 |
| A. | A | B. | B | C. | C | D. | D |

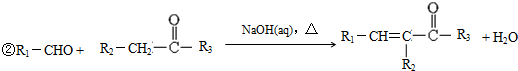
 .
.
 .
.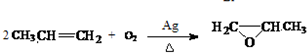 .
. .
. .
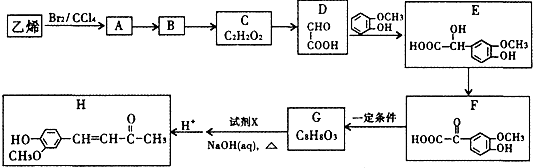
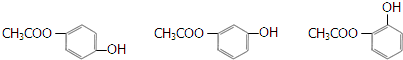
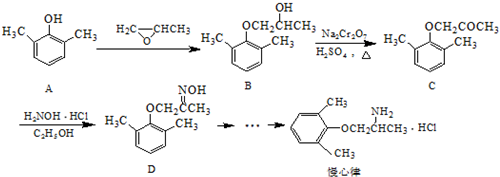
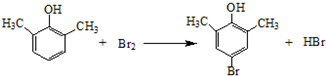
.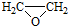 ).写出以邻甲基苯酚 (
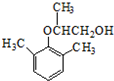
).写出以邻甲基苯酚 (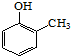 )和乙醇为原料制备
)和乙醇为原料制备 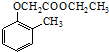 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:CH3CH2OH$→_{170℃}^{浓H_{2}SO_{4}}$CH2=CH2.
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:CH3CH2OH$→_{170℃}^{浓H_{2}SO_{4}}$CH2=CH2.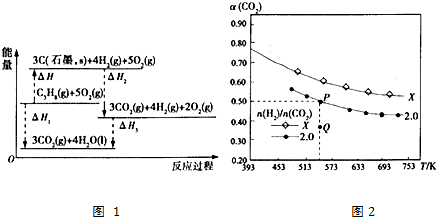
 利用2Al+2NaOH+2H2O=2NaAlO2+3H2反应,设计一个原电池.
利用2Al+2NaOH+2H2O=2NaAlO2+3H2反应,设计一个原电池.