题目内容
(8分)1808年,英国化学家用钾还原氧化镁,最早制得少量的镁。镁是航空工业的重要材料,镁作为一种强还原剂,还用于钛、铍和铀的生产中。
(1)镁在元素周期表中的位置为 。
(2)写出用镁与金红石(主要成分为TiO2)在加热条件下制取钛的化学方程式:
。
(3)镁在加热的条件下还能与NaOH固体反应,生成MgO和单质X、单质Y。已知X与水反应可生成单质Y,则镁与NaOH反应的化学方程式为: 。
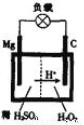
(4)镁一过氧化氢电池的工作原理如图所示,该电池放电时总反应的化
学方程式为:
(1)第三周期IIA族
(2)2Mg+TiO2 Ti+2MgO
Ti+2MgO
(3)2 Mg+2NaOH 2MgO+2Na+H2↑
2MgO+2Na+H2↑
(4)Mg+H2O2+H2SO4=MgSO4+2H2O
【解析】
试题分析:(1)Mg在元素周期表中位于第三周期IIA族;
(2)Mg与TiO2加入条件下发生氧化还原反应,生成氧化镁与Ti,化学方程式为2Mg+TiO2 Ti+2MgO
Ti+2MgO
(3)根据元素守恒,Mg与NaOH固体加热时生成氧化镁,同时还有2种单质,则2种单质是Na和H2,Na与水反应生成氢气,所以化学方程式为2 Mg+2NaOH 2MgO+2Na+H2↑
2MgO+2Na+H2↑
(4)镁一过氧化氢电池中Mg只能做还原剂,而过氧化氢则是氧化剂,所以Mg失去电子生成Mg2+,而H2O2中O元素的化合价降低生成水,则总反应的方程式为Mg+H2O2+H2SO4=MgSO4+2H2O
考点:考查化学方程式的书写,元素位置的判断

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
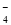 、
、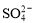
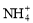 、K+、
、K+、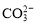
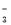 、Cl-
、Cl- 4NO(g)+ 6H2O(g),下列叙述正确的是
4NO(g)+ 6H2O(g),下列叙述正确的是 与80%的硫酸反应可生成
与80%的硫酸反应可生成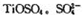 的空间构型为 形,其中硫原子采用 杂化。
的空间构型为 形,其中硫原子采用 杂化。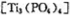 锂离子电池能来那个密度大、安全性高。
锂离子电池能来那个密度大、安全性高。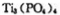 可由
可由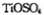 与
与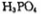 反应制得。两分子
反应制得。两分子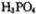 发生脱水生成焦磷酸:
发生脱水生成焦磷酸: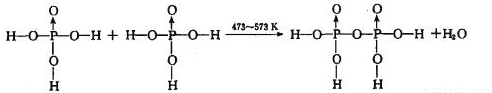
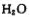 生成三磷酸,其结构式为 ,四分子
生成三磷酸,其结构式为 ,四分子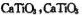 的晶体结构如图所示(Ti位于立方体的顶点)。该晶体中Ti4+和周围 个O2-紧邻。
的晶体结构如图所示(Ti位于立方体的顶点)。该晶体中Ti4+和周围 个O2-紧邻。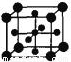
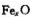 (x<1),若测得某
(x<1),若测得某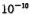 m,则
m,则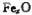 中x= 。
中x= 。
 、NO
、NO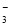
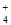 、Na+、SiO
、Na+、SiO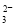 、HCO
、HCO