题目内容
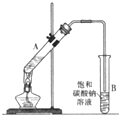 乙酸乙酯是重要的化工原料.实验室合成乙酸乙酯的装置如图所示.
乙酸乙酯是重要的化工原料.实验室合成乙酸乙酯的装置如图所示.有关数据及副反应:
| 乙酸 | 乙醇 | 乙酸乙酯 | 乙醚 | |
| 沸点/℃ | 118 | 78.3 | 77.1 | 34.5 |
| 溶解性 | 易溶于水 | 与水混溶 | 与乙醚混溶 | 微溶于水 |
| 浓硫酸 |
| 140℃ |
请回答下列问题:
(1)在大试管A中添加的试剂有6mL乙醇、4mL乙酸和4mL浓硫酸,这三种试剂添加顺序依次为
(2)试管B中饱和碳酸钠溶液的作用是
(3)现对试管B中乙酸乙酯粗产品进行提纯,步骤如下:
①将试管B中混合液体充分振荡后,转入
②向分离出的上层液体中加入无水硫酸钠,充分振荡.加入无水硫酸钠的目的是:
③将经过上述处理的液体放入干燥的蒸馏烧瓶中,对其进行蒸馏,收集
(4)从绿色化学的角度分析,使用浓硫酸制乙酸乙酯不足之处主要有
考点:乙酸乙酯的制取
专题:实验题
分析:(1)为防止酸液飞溅,应先加入乙醇,然后在加入浓硫酸和乙酸;
(2)用饱和碳酸钠溶液吸收乙酸乙酯,乙醇溶解,碳酸钠与乙酸反应除去乙酸、同时降低乙酸乙酯的溶解度;
(3)根据乙酸乙酯不溶于饱和碳酸钠,采用分液的方法分离,再用无水硫酸钠除去乙酸乙酯中的水,最后蒸馏可得纯净的乙酸乙酯;
(4)反应需要浓硫酸作催化剂,产生酸性废水,同时乙醇发生副反应.
(2)用饱和碳酸钠溶液吸收乙酸乙酯,乙醇溶解,碳酸钠与乙酸反应除去乙酸、同时降低乙酸乙酯的溶解度;
(3)根据乙酸乙酯不溶于饱和碳酸钠,采用分液的方法分离,再用无水硫酸钠除去乙酸乙酯中的水,最后蒸馏可得纯净的乙酸乙酯;
(4)反应需要浓硫酸作催化剂,产生酸性废水,同时乙醇发生副反应.
解答:
解:(1)制取乙酸乙酯时,应先加入乙醇,然后在加入浓硫酸和乙酸,如先加浓硫酸会出现酸液飞溅,
故答案为:6 mL乙醇 4 mL浓硫酸 4 mL乙酸;
(2)制备乙酸乙酯时常用饱和碳酸钠溶液吸收乙酸乙酯,目的是除去乙醇和乙酸、降低乙酸乙酯的溶解度,便于分层.
故答案为:除去乙醇和乙酸、降低乙酸乙酯的溶解度,便于分层;
(3)乙酸乙酯不溶于饱和碳酸钠,采用分液的方法分离,需要分液漏斗,再用无水硫酸钠除去乙酸乙酯中的水,蒸馏时收集77℃左右的液体即得纯净的乙酸乙酯;
故答案为:分液漏斗;除去乙酸乙酯中的水;77.1;
(4)反应需要浓硫酸作催化剂,产生酸性废水,同时乙醇发生副反应产生大量污染物;
故答案为:产生酸性废水,污染环境,同时发生副反,产生大量污染物.
故答案为:6 mL乙醇 4 mL浓硫酸 4 mL乙酸;
(2)制备乙酸乙酯时常用饱和碳酸钠溶液吸收乙酸乙酯,目的是除去乙醇和乙酸、降低乙酸乙酯的溶解度,便于分层.
故答案为:除去乙醇和乙酸、降低乙酸乙酯的溶解度,便于分层;
(3)乙酸乙酯不溶于饱和碳酸钠,采用分液的方法分离,需要分液漏斗,再用无水硫酸钠除去乙酸乙酯中的水,蒸馏时收集77℃左右的液体即得纯净的乙酸乙酯;
故答案为:分液漏斗;除去乙酸乙酯中的水;77.1;
(4)反应需要浓硫酸作催化剂,产生酸性废水,同时乙醇发生副反应产生大量污染物;
故答案为:产生酸性废水,污染环境,同时发生副反,产生大量污染物.
点评:本题考查了酯化反应,掌握混合物的分离和提纯方法,明确实验的实验原理是解答该题的关键,题目难度不大.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
已知热化学方程式:2SO2(g)+O2(g)?2SO3(g)△H=-Q kJ?mol-1(Q>0).下列说法正确的是( )
| A、相同条件下,2 mol SO2(g)和1 mol O2(g)所具有的能量小于2 mol SO3(g)所具有的能量 |
| B、将2 mol SO2(g)和1 mol O2(g)置于一密闭容器中充分反应后,放出热量为Q kJ |
| C、增大压强或升高温度,该反应过程放出更多的热量 |
| D、如将一定量SO2(g)和O2(g)置于某密闭容器中充分反应后放热Q kJ,则此过程中有2 mol SO2(g)被氧化 |
铜粉放入稀硫酸溶液中,加热后无明显变化,但加入下列某试剂一段时间后,发现铜粉质量减少,溶液呈蓝色.加入试剂:①FeCl2;②Na2CO3;③KNO3;④FeSO4;⑤FeCl3;⑥H2O2;⑦NaClO;⑧NaOH.则该试剂可能是( )
| A、①④⑤ | B、②③⑦⑧ |
| C、③⑤⑥⑦ | D、全部 |
下列实验装置正确的是( )
A、 收集SO2气体 |
B、 制取并收集O2 |
C、 检验溴乙烷与NaOH醇溶液共热产生的C2H4 |
D、 从食盐水中提取NaCl |

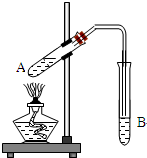 某同学在实验室用下图所示实验装置制取乙酸乙酯.回答下列问题:
某同学在实验室用下图所示实验装置制取乙酸乙酯.回答下列问题: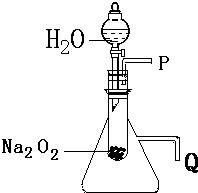 用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,向脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来.
用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,向脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来.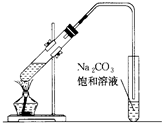 如图是实验室制乙酸乙酯的装置.
如图是实验室制乙酸乙酯的装置.