题目内容
5.水的电离平衡曲线如图所示,根据图中数据,回答下列问题: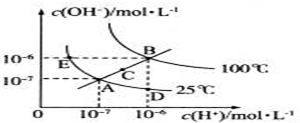
(1)图中A、B、C、D四点的KW 由大到小的顺序:B>C>A=D.
(2)若从A点到E点,可采用的方法是加入活泼金属钠.
(3)在100℃时,将pH=2的硫酸与pH=12的KOH溶液混合至呈中性,需硫酸和氢氧化钾的体积比为100:1.
(4)pH=12的氢氧化钠溶液温度由25℃高到100℃,pH=10.
分析 (1)A、D、E都处于25℃时,Kw相等,然后比较B、E两点的c(H+)和c(OH-)的大小,依次比较Kw的大小;
(2)从A点到E点c(H+)变小,但c(OH-)变大,温度不变,Kw不变;
(3)根据B点时Kw计算酸与碱溶液中c(H+)和c(OH-),然后判断溶液的酸碱性;
(4)pH=12的氢氧化钠溶液温度由25℃时氢氧根离子的浓度为:10-2mol/L,而100℃时水的离子积常数为:10-12,所以此温度下氢离子的浓度为:10-10mol/L.
解答 解:(1)A、D、E都处于25℃时,Kw相等,B点c(H+)和c(OH-)都大于E点的c(H+)和c(OH-),并且E点的c(H+)和c(OH-)大于A点c(H+)和c(OH-),c(H+)和c(OH-)越大,Kw越大,故B>C>A=D=,故答案为:B>C>A=D;
(2)若从A点到E点,可采用的方法是加入活泼金属钠,使c(H+)变小,但c(OH-)变大,故答案为:加入活泼金属钠;
(3)若处在B点时,pH=2的硫酸中c(H+)=10-2mol/L,pH=12的KOH中c(OH-)=1mol/L,溶液显中性,故需硫酸月氢氧化钾的比值为100:1,故答案为:100:1;
(4)pH=12的氢氧化钠溶液温度由25℃时氢氧根离子的浓度为:10-2mol/L,而100℃时水的离子积常数为:10-12,所以此温度下氢离子的浓度为:10-10mol/L,则PH=10,故答案为:10.
点评 本题考查了酸碱混合的定性判断、弱电解质电离、PH的计算,题目难度较大,试题涉及知识点较多、综合性较强,需要弱电解质的电离特点分析解答,注意平衡常数只与温度有关,与溶液酸碱性、离子浓度定性无关,为易错点.

练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目
8.下列反应的离子方程式书写正确的是( )
| A. | MgO溶于稀盐酸中:O2-+2H+═H2O | |
| B. | 碳酸钙中滴加稀盐酸:CO32-+2H+═CO2↑+H2O | |
| C. | 实验室用MnO2反应制Cl2:MnO2+2H++2Cl-═Cl2↑+Mn2++H2O | |
| D. | 向氢氧化钠溶液中通入过量二氧化碳:OH-+CO2=HCO3- |
9.现有如下反应热信息
下列说法正确的是( )
| 热化学方程式 | △H |
| 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(1) | -2600 kJ•mol-1 |
| 2C6H6(g)+15O2(g)═12CO2(g)+6H2O(1) | -6590 kJ•mol-1 |
| 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(g) | -a kJ•mol-1 |
| 2C6H6(1)+15O2(g)═12CO2(g)+6H2O(1) | -b kJ•mol-1 |
| A. | a>2600 | |
| B. | b>6590 | |
| C. | 相同条件下,等质量的C2H2(g)与C6H6(g)完全燃烧,C2H2(g)放热更多 | |
| D. | C2H2(g)三聚生成C6H6(g)的过程属于吸热反应 |
13.下列叙述正确的是( )
| A. | 1molH2O的质量为18g/mol | B. | CH4的摩尔质量为16g | ||
| C. | 1mol任何气体体积均为22.4L | D. | 0.5molSO2分子的质量为32g |
10.下列各组离子水溶液中能大量共存的是( )
| A. | I-、ClO-、NO3-、H+ | B. | Fe3+、Cu2+、SO42-、Cl- | ||
| C. | H+、K+、AlO2-、HSO3- | D. | Ca2+、Na+、SO42-、CO32- |
14.某一元弱酸HA的相对分子质量为M.在t℃时,将ag HA完全溶解于水中,得V mL饱和溶液,测得该溶液的密度为ρ g/cm3,其中溶液pH=b.下列叙述中,错误的是( )
| A. | t℃时,HA的Ka=10-2b/1000a/MV | |
| B. | 物质的量浓度:c(HA)=1000a/MV mol•L-1 | |
| C. | t℃时,HA的溶解度:S=100a/ρV g | |
| D. | HA的质量分数:ω(HA)=(a/ρV)×100% |
15.一定条件下反应N2+3H2?2NH3达平衡,当单独改变下述条件后有关叙述一定错误的是( )
| A. | 加催化剂,v(正)和v(逆)都发生变化,且变化的倍数相等 | |
| B. | 加压,v(正)和v(逆)都增大,且v(正)增加倍数大于v(逆)增加倍数 | |
| C. | 降温,v(正)和v(逆)都减少,且v(正)减少倍数大于v(逆)减少倍数 | |
| D. | 增加c(N2),v(正)和v(逆)都增大,且v(正)增加倍数大于v(逆)增加倍数 |

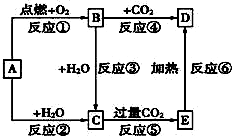 如图中,A为一种常见的单质,B、C、D、E是含有A元素的常见化合物.已知A在空气中燃烧生成淡黄色固体(部分产物已略去).
如图中,A为一种常见的单质,B、C、D、E是含有A元素的常见化合物.已知A在空气中燃烧生成淡黄色固体(部分产物已略去).