题目内容
现有标准状况下四种气体:①5.6LH2S ②0.6molNH3 ③6gC2H6 ④8gCH4,按要求将他们由大到小排列(填写序号)
(1)体积
(2)质量
(3)氢原子数
(4)密度 .
(1)体积
(2)质量
(3)氢原子数
(4)密度
考点:气体摩尔体积,物质的量的相关计算
专题:阿伏加德罗常数和阿伏加德罗定律
分析:根据n=
=
=
计算各物质的物质的量,同温同压下,体积之比等于物质的量之比;结合分子式计算氢原子的物质的量;同温同压下,密度之比等于其摩尔质量之比;根据m=nM计算各物质的质量,据此进行判断.
| m |
| M |
| V |
| Vm |
| N |
| NA |
解答:
解:现有标准状况下四种气体:①5.6LH2S ②0.6molNH3 ③6gC2H6 ④8gCH4,分别计算物质的量得到
①5.6LH2S 物质的量=
=0.25mol,②0.6molNH3 ③6gC2H6 物质的量=
=0.2mol,④8gCH4物质的量=
=0.5mol
(1)相同条件下,气体的体积之比等于物质的量之比,所以体积体积②>④>①>③;
故答案为:②>④>①>③;
(2)各物质的质量分别为:①5.6LH2S 为0.25mol×34g/mol=8.5g,②0.6molNH3 为0.6mol×17g/mol=10.2g,③6gC2H6,④8gCH4,所以质量②>①>④>③;
故答案为:②>①>④>③;
(3)各物质中H原子的物质的量分别为:①H2S 含有H原子为0.25mol×2=0.5mol,②0.6molNH3 中含有H原子为 0.6mol×3=1.8mol,③0.2molC2H6中含有氢原子为0.2mol×6=1.2mol,④0.5molCH4 中含有H原子为0.5mol×4=2mol,所以氢原子个数④>②>③>①;
故答案为:④>②>③>①;
(4)各物质的摩尔质量分别为:①H2S 为34g/mol,②NH3为17g/mol,③C2H6的摩尔质量为30g/mol,④CH4 为16g/mol,相同条件下,密度之比等于摩尔质量之比,所以密度①>③>②>④;
故答案为:①>③>②>④.
①5.6LH2S 物质的量=
| 5.6L |
| 22.4L/mol |
| 6g |
| 30g/mol |
| 8g |
| 16g/mol |
(1)相同条件下,气体的体积之比等于物质的量之比,所以体积体积②>④>①>③;
故答案为:②>④>①>③;
(2)各物质的质量分别为:①5.6LH2S 为0.25mol×34g/mol=8.5g,②0.6molNH3 为0.6mol×17g/mol=10.2g,③6gC2H6,④8gCH4,所以质量②>①>④>③;
故答案为:②>①>④>③;
(3)各物质中H原子的物质的量分别为:①H2S 含有H原子为0.25mol×2=0.5mol,②0.6molNH3 中含有H原子为 0.6mol×3=1.8mol,③0.2molC2H6中含有氢原子为0.2mol×6=1.2mol,④0.5molCH4 中含有H原子为0.5mol×4=2mol,所以氢原子个数④>②>③>①;
故答案为:④>②>③>①;
(4)各物质的摩尔质量分别为:①H2S 为34g/mol,②NH3为17g/mol,③C2H6的摩尔质量为30g/mol,④CH4 为16g/mol,相同条件下,密度之比等于摩尔质量之比,所以密度①>③>②>④;
故答案为:①>③>②>④.
点评:本题考查了物质的量的有关计算,注意把握有关公式的应用,题目难度不大.

练习册系列答案
相关题目
下列十二种物质中:Fe、CaO、SO3、盐酸、硫酸、KOH溶液、NH4HCO3、CCl4、NH3?H2O、HF、BaSO4、熔融的KCl.其中属于强电解质、弱电解质、非电解质的物质种类依次为( )
| A、5、2、2 |
| B、7、3、2 |
| C、6、2、4 |
| D、5、3、4 |
下列说法不正确的是( )
| A、在自然界中存在的单质,一定具备化学性质稳定、不与其它物质发生反应这一特征 |
| B、100多年前,英国曾耗巨资改建高炉,试图延长CO和Fe2O3的接触时间,以减少CO的排放,这违背了化学反应都有一定限度这一基本原理 |
| C、在溶液中,有色物质参与的反应,可以用分光光度计来测定其化学反应速率 |
| D、虽然碳酸钙分解需要吸收大量的热,但在高温条件下也能自发进行 |
下列离子方程式与所述事实相符且正确的是( )
| A、向NaClO溶液中通入少量二氧化硫 3ClO-+SO2+H2O═2HClO+SO42-+Cl- |
| B、碳酸氢钙与过量的NaOH溶液反应Ca2++HCO3-+OH-═CaCO3↓+H2O |
| C、用二氧化硫水溶液吸收溴蒸气:SO2+Br2+2H2O═SO42-+2H++2HBr |
| D、在碳酸氢铵稀溶液中加入足量的氢氧化钠稀溶液:NH4++OH-═NH3?H2O |
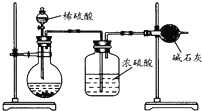 为了测定氢氧化钠和碳酸钠固体混合物中碳酸钠的质量分数,甲、乙两位同学分别设计了如下的实验方案:
为了测定氢氧化钠和碳酸钠固体混合物中碳酸钠的质量分数,甲、乙两位同学分别设计了如下的实验方案: