题目内容
13.下列离子方程式表达正确的是( )| A. | AgNO3溶液中加入过量的氨水:Ag++NH3•H2O=AgOH↓+NH4+ | |
| B. | 铵明矾[NH4Al(SO4)2•12H2O]溶液中加入过量Ba(OH)2溶液:Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O | |
| C. | H2O2溶液中滴加酸性KMnO4溶液:2 MnO4-+5 H2O2+6H+=2Mn2++5O2↑+8H2O | |
| D. | 尼泊金酸(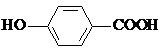 )与碳酸氢钠溶液反应: )与碳酸氢钠溶液反应: |
分析 A.向AgNO3溶液中逐滴加入过量氨水,先生成氢氧化银白色沉淀,后生成氢氧化银氨溶液;
B.硫酸铝铵电离产生的氨根离子和铝离子都能够与氢氧根离子反应,铝离子先与氢氧根离子反应生成氢氧化铝,同时发生反应为SO42-+Ba2+=BaSO4↓,然后氨根离子与氢氧根离子反应生成一水合氨,继续滴加碱,氢氧根离子与生成的氢氧化铝沉淀反应生成偏铝酸盐;
C.H2O2与酸性KMnO4溶液反应放出锰离子、氧气和水;
D.尼泊金酸中,只有羧基的酸性比碳酸酸性强,能和碳酸氢根离子反应.
解答 解:A.向AgNO3溶液中逐滴加入氨水,开始会生成氢氧化银白色沉淀,但是氢氧化银会溶于过量的氨水中,反应生成氢氧化银氨溶液,会出现沉淀然后消失,离子方程式为:Ag++3NH3•H2O=Ag(NH3)2OH↓+NH4++2H2O,故A错误;
B.NH4Al(SO4)2•12H2O和Ba(OH)2 按照1:2恰好反应生成硫酸钡沉淀、氢氧化铝沉淀、一水合氨,继续加入氢氧化钡,氢氧化铝沉淀完全溶解,反应的离子方程式为:NH4++Al3++2SO42-+2Ba2++5OH-=2BaSO4↓+NH3•H2O+AlO2-+2H2O,故B错误;
C.H2O2与酸性KMnO4溶液反应放出锰离子氧气和水,反应的离子方程式为:5H2O2+2MnO4-+6H+=2Mn2++5O2↑+8H2O,故C正确;
D.只有羧基的酸性比碳酸酸性强,与尼泊金酸反应,正确的离子方程式为 HOC6H4COOH+NaHCO3→HOC6H4COONa+CO2↑+H2O,故D错误;
故选C.
点评 本题考查了离子方程式的书写方法和注意问题,主要是反应产物判断,原子守恒、电子守恒、电荷守恒分析应用,注意离子反应顺序是解题关键,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.已知某有机物的结构如图所示,下列说法正确的是( )
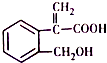

| A. | 分子式为C10H10O3 | |
| B. | 1mol 该有机物最多可与5mol氢气发生加成反应 | |
| C. | 该有机物在一定条件下,可以发生取代、氧化、消去反应 | |
| D. | 1mol 该有机物与足量钠反应生成22.4L氢气(标况下) |
4.在强酸性溶液中能够大量共存的离子组是( )
| A. | Na+、Cl-、Al3+、Ag+ | B. | $NH_4^+$、Mg2+、$NO_3^-$、$SO_4^{2-}$ | ||
| C. | K+、Ca2+、$NO_3^-$、$CO_3^{2-}$ | D. | $HCO_3^-$、Na+、K+、$SO_4^{2-}$ |
5.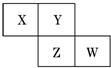 X、Y、Z、W均为短周期元素,它们在元素周期表中的相对位置如图所示.若Z原子的最外层电子数是第一层电子数的3倍,下列说法中正确的是( )
X、Y、Z、W均为短周期元素,它们在元素周期表中的相对位置如图所示.若Z原子的最外层电子数是第一层电子数的3倍,下列说法中正确的是( )
 X、Y、Z、W均为短周期元素,它们在元素周期表中的相对位置如图所示.若Z原子的最外层电子数是第一层电子数的3倍,下列说法中正确的是( )
X、Y、Z、W均为短周期元素,它们在元素周期表中的相对位置如图所示.若Z原子的最外层电子数是第一层电子数的3倍,下列说法中正确的是( )| A. | X的最常见气态氢化物的水溶液显酸性 | |
| B. | 最高价氧化物对应水化物的酸性W比Z强 | |
| C. | Z的单质与氢气反应比Y单质与氢气反应剧烈 | |
| D. | X的原子半径小于Y |
2.下列说法或推理正确的是( )
| A. | 将Fe(N03)2样品溶于稀H2SO4后,滴加KSCN溶液,溶液变红,则Fe(N03)2晶体已氧化变质 | |
| B. | 常温下,pH都为11的氢氧化钠溶液和氨水均加水稀释100倍,pH都变为9 | |
| C. | 25℃时,Ksp( BaC03)>Ksp( BaCrO4),则沉淀水体中的Ba2+选择Na2CrO4比Na2CO3好 | |
| D. | 将CH3CH2Br与NaOH溶液共热,冷却后取出上层溶液,加入AgNO3溶液,产生沉淀,则CH3CH2Br在NaOH溶液中发生了水解 |
3.下列气体通入水中,水溶液呈碱性的是( )
| A. | NH3 | B. | NO | C. | SO3 | D. | CO2 |