题目内容
18.已知14.2g X气体的物质的量为0.2mol,则X气体的摩尔质量是( )| A. | 71g | B. | 71 | C. | 71g/mol | D. | 142g/mol |
分析 结合M=$\frac{m}{n}$计算.
解答 解:14.2g X气体的物质的量为0.2mol,则X气体的摩尔质量是$\frac{14.2g}{0.2mol}$=71g/mol,
故选C.
点评 本题考查物质的量的计算,为高频考点,把握物质的量与质量、摩尔质量为解答的关键,侧重分析与计算能力的考查,注意摩尔质量的单位,题目难度不大.

练习册系列答案
 小学期末标准试卷系列答案
小学期末标准试卷系列答案
相关题目
8.下列反应不属于四种基本反应类型,但属于氧化还原反应的( )
| A. | 2K+2H2O=2KOH+H2↑ | B. | Cu(NO3)2+2NaOH=Cu(OH)2↓+2NaNO3 | ||
| C. | 2Cu(NO3)2=2CuO+4NO2↑+O2↑ | D. | 3CO+Fe2O3=2Fe+3CO2 |
6.下列反应方程式中有一个与其他三个在分类上不同,这个反应是( )
| A. | 3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4 | B. | CO2+C$\frac{\underline{\;\;△\;\;}}{\;}$2CO | ||
| C. | NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O↑+CO2↑ | D. | CaCO3+CO2+H2O═Ca(HCO3)2 |
13.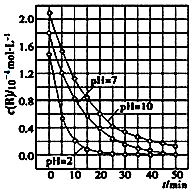 二氧化钛在一定波长光的照射下,可有效降解甲醛、苯等有机物,效果持久,且自身对人体无害.某课题组研究了溶液的酸碱性对TiO2光催化染料R降解反应的影响,结果如图所示.下列判断正确的是( )
二氧化钛在一定波长光的照射下,可有效降解甲醛、苯等有机物,效果持久,且自身对人体无害.某课题组研究了溶液的酸碱性对TiO2光催化染料R降解反应的影响,结果如图所示.下列判断正确的是( )
 二氧化钛在一定波长光的照射下,可有效降解甲醛、苯等有机物,效果持久,且自身对人体无害.某课题组研究了溶液的酸碱性对TiO2光催化染料R降解反应的影响,结果如图所示.下列判断正确的是( )
二氧化钛在一定波长光的照射下,可有效降解甲醛、苯等有机物,效果持久,且自身对人体无害.某课题组研究了溶液的酸碱性对TiO2光催化染料R降解反应的影响,结果如图所示.下列判断正确的是( )| A. | 在0~50 min之间,R的降解百分率pH=2大于pH=7 | |
| B. | 溶液酸性越强,R的降解速率越大 | |
| C. | R的起始浓度不同,无法判断溶液的酸碱性对R的降解速率的影响 | |
| D. | 在20~25 min之间,pH=10时R的降解速率为04mol•L-1•min-1 |
3.将Na、Mg、Al各0.4mol分别放入100mL、2mol/L的盐酸中,同温同压下产生的气体的体积比是( )
| A. | 1:1:1 | B. | 2:1:1 | C. | 3:1:1 | D. | 1:2:3 |
7.下列图中所示的实验操作评价合理的是( )
| A. | 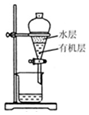 用如图装置分离有机 层与水层,水层从分液 漏斗下口放出 | |
| B. | 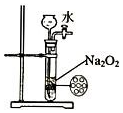 用如图装置可用来制 备少量氧气,并且控制 反应的发生与停止 | |
| C. | 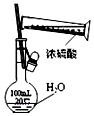 如图中配制一定物质的量浓度的硫酸溶液不能 直接在容量瓶中进行 | |
| D. | 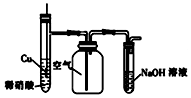 用如图装置制备并收集NO气体 |
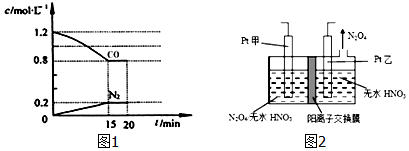
 .
.