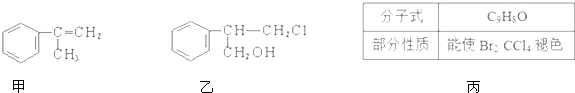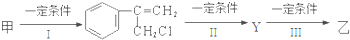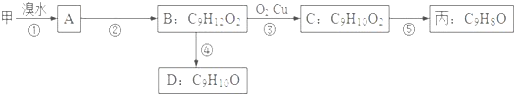题目内容
用湿润的淀粉碘化钾试纸检验氯气现象是 .
考点:氯气的化学性质
专题:
分析:氯气具有强氧化性,能和碘离子反应生成碘单质,碘遇淀粉试液变蓝色,据此分析解答.
解答:
解:氯气具有强氧化性,能和碘离子发生氧化还原反应生成碘单质,Cl2+2I-=I2+2Cl-,碘遇淀粉试液变蓝色,所以看到的现象是:无色湿润的淀粉碘化钾试纸变蓝色,故答案为:无色湿润的淀粉碘化钾试纸变蓝色.
点评:本题考查氯气、碘的性质,侧重考查氧化还原反应、物质的检验,明确物质性质是解本题关键,会运用化学语言解释实验现象,题目难度不大.

练习册系列答案
相关题目
金属钒被誉为“合金的维生素”.五氧化二钒(V2O5)中钒元素的化合价为( )
| A、-3 | B、+1 | C、+3 | D、+5 |
下列水溶液中的各组离子能大量共存的是( )
| A、Na+、Ba2+、Cl-、SO42- |
| B、Ca2+、NO3-、C1-、K+ |
| C、Cu2+、K+、OH-、Cl- |
| D、H+、Cl-、Na+、CO32- |
影响化学反应速率的因素有多方面,如浓度.压强.温度.催化剂等.下列有关说法不正确的是( )
| A、改变压强能改变气体反应的速率 |
| B、增大浓度能加快化学反应速率,原因是增大浓度就增加了反应体系中活化分子的百分数 |
| C、温度升高使化学反应速率加快的主要原因是增加了反应体系中活化分子的百分数 |
| D、催化剂能加快化学反应速率主要原因是降低反应所需的能量 |
下列反应的离子方程式不正确的是( )
| A、铁与氯化铁溶液:2Fe3++Fe═3Fe2+ |
| B、氯气与溴化钠溶液:2Br-+Cl2═Br2+2Cl- |
| C、硫酸铵和氢氧化钡溶液:Ba2++SO42-═BaSO4↓ |
| D、铜与稀硝酸:3Cu+8H++2NO3-═Cu2++2NO↑+4H2O |
下列说法正确的是( )
| A、将AlCl3溶液和Al2(SO4)3溶液分别加热、蒸干、灼烧,所得固体成分相同 |
| B、配制FeSO4溶液时,将FeSO4固体溶于稀盐酸中,然后稀释至所需浓度 |
| C、用加热的方法可以除去KCl溶液中的Fe3+ |
| D、洗涤油污常用热的碳酸钠溶液 |
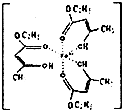 氯化铁溶液用于检验食用香精乙酰乙酸乙酯时,会生成紫色配合物,其配离子结构如图所示.
氯化铁溶液用于检验食用香精乙酰乙酸乙酯时,会生成紫色配合物,其配离子结构如图所示.