题目内容
下列有关化学用语表达正确的是( )
A、NH4Cl的电子式: | ||
B、氚表示为
| ||
| C、次氯酸的结构式为H-O-Cl | ||
| D、16O2和18O2互为同素异形体 |
考点:电子式、化学式或化学符号及名称的综合,同位素及其应用,同素异形体
专题:
分析:A.铵根离子为复杂阳离子,没有表示出N、H原子的最外层电子;
B.氚的质量数为3,元素符号应该H表示;
C.次氯酸分子的中心原子为O原子,分子中存在1个氢氧键和1个氧氯键;
D.同素异形体为同种元素形成的不同单质,二者都是氧气,为同一种物质.
B.氚的质量数为3,元素符号应该H表示;
C.次氯酸分子的中心原子为O原子,分子中存在1个氢氧键和1个氧氯键;
D.同素异形体为同种元素形成的不同单质,二者都是氧气,为同一种物质.
解答:
解:A.氯化铵为离子化合物,铵根离子需要标出其原子的最外层电子,氯化铵正确的电子式为: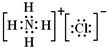 ,故A错误;
,故A错误;
B.氚的质量数为3、质子数为1,该原子可以表示为:31H,故B错误;
C.次氯酸分子中存在1个氢氧键和1个氧氯键,其结构式为:H-O-Cl,故C正确;
D.16O2和18O2都是氧气分子,为同一种物质,不属于同素异形体,故D错误;
故选C.
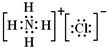 ,故A错误;
,故A错误;B.氚的质量数为3、质子数为1,该原子可以表示为:31H,故B错误;
C.次氯酸分子中存在1个氢氧键和1个氧氯键,其结构式为:H-O-Cl,故C正确;
D.16O2和18O2都是氧气分子,为同一种物质,不属于同素异形体,故D错误;
故选C.
点评:本题考查了化学用语的判断,题目难度中等,注意掌握常见化学用语的概念及表示方法,明确离子化合物与共价化合物的电子式的区别,明确同素异形体与同位素的概念.

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案
相关题目
元素的原子结构决定其性质和在周期表中的位置,下列说法正确的是( )
| A、元素周期表中位于金属和非金属分界线附近的元素过渡元素 |
| B、氯化氢和氯化钠于水需克服相同类型的作用力 |
| C、Ba(OH)2的碱性比Mg(OH)2的碱性强 |
| D、离子半径:O2->Na+ |
下列说法正确的是( )
| A、通过电解氯化钠水溶液可制得金属钠和氯气 |
| B、氯化铁溶液能腐蚀铜制容器 |
| C、在食品袋中放置盛有铁粉、碳、氯化钠等物质的透气小袋,可防止食物氧化变质 |
| D、点燃的镁条伸入二氧化碳气体会氮气中都能继续燃烧 |
 电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图如图,其中电解池中隔膜仅阻止气体通过,阴、阳极均为石墨电极.下列相关叙述正确的是( )
电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图如图,其中电解池中隔膜仅阻止气体通过,阴、阳极均为石墨电极.下列相关叙述正确的是( )| A、b电极为阳极 |
| B、电子由b电极经过溶液流入a电极形成回路 |
| C、b电极上发生失去电子的反应 |
| D、尿素在a电极发生氧化反应 |
肼(N2H4)又称联氨,可用如下方法制备:CO(NH2)2+ClO-+OH--N2H4+Cl-+CO32-+H2O,[CO(NH2)]2中N为-3价,方程式未配平],下列说法不正确的是( )
| A、N2H4是氧化产物 |
| B、N2H4中存在极性键和非极性键 |
| C、配平后,OH-的化学计量数为2 |
| D、生成3.2 g N2H4转移0.1 mol电子 |
下列表达正确的是( )
A、氟原子中能量最髙的电子其电子云图: |
B、CO2的分子模型示意图: |
C、2-甲基丁醛的结构简式: |
D、N2的结构式: |
下列反应的离子方程式正确的是( )
A、二氧化锰和浓盐酸制取氯气:MnO2+4H+=2Cl-
| ||||
| B、碳酸钠溶液用作洗涤剂的原理:CO32-+2H2O?H2CO3+2OH- | ||||
| C、用氯化铁溶液与铜反应制作印刷电路板:Fe3++Cu═Fe2++Cu2+ | ||||
| D、氯化铝溶液与氨水制取氢氧化铝:Al3++3OH-═Al(OH)3↓ |
 莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中.下列关于这两种有机化合物的说法正确的是( )
莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中.下列关于这两种有机化合物的说法正确的是( )| A、两种酸都能与溴水反应 |
| B、两种酸遇三氯化铁溶液都显色 |
| C、鞣酸分子与莽草酸分子相比多了两个碳碳双键 |
| D、中和等物质的量的两种酸消耗的氢氧化钠的量相同 |
 25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq)?Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示.下列判断正确的是( )
25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq)?Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示.下列判断正确的是( )| A、往平衡体系中加入金属铅后,c(Pb2+)增大 |
| B、往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变大 |
| C、升高温度,平衡体系中c(Pb2+)增大,说明该反应△H>0 |
| D、25℃时,该反应的平衡常数K=0.22 |