题目内容
碘化钠是无色立方晶体或白色结晶性粉末,其水溶液呈微碱性,具有还原性、潮解性,在潮湿空气中因吸收水分而结块.碘化钠与空气接触,能使碘游离析出,工业上常用铁屑还原法来制备碘化钠,同时可得到副产品.工艺流程如图所示:

(1)反应①中氧化产物与还原产物的物质的量之比为 .
(2)判断反应①中的碘是否已完全转化的具体操作方法是 .
(3)向NaIO3溶液中加入铁屑的目的是 ,反应②的离子方程式为 .
(4)在将滤液浓缩、冷却结晶、分离、干燥和包装过程中,都需要注意的问题是 .

(1)反应①中氧化产物与还原产物的物质的量之比为
(2)判断反应①中的碘是否已完全转化的具体操作方法是
(3)向NaIO3溶液中加入铁屑的目的是
(4)在将滤液浓缩、冷却结晶、分离、干燥和包装过程中,都需要注意的问题是
考点:制备实验方案的设计,氯、溴、碘及其化合物的综合应用
专题:实验设计题
分析:由制备流程可知,碘与NaOH溶液反应生成NaI、NaIO3,加入Fe与NaIO3发生氧化还原反应生成NaI、氢氧化铁,经过滤后得到固体氢氧化亚铁,过滤后溶液中主要含NaI,分离、提纯得到NaI,以此来解答.
解答:
解:由制备流程可知,碘与NaOH溶液反应生成NaI、NaIO3,加入Fe与NaIO3发生氧化还原反应生成NaI、氢氧化铁,经过滤后得到固体氢氧化铁,过滤后溶液中主要含NaI,分离、提纯得到NaI,
(1)反应①为碘单质和氢氧化钠溶液的反应生成碘化钠,碘酸钠和水,3I2+6NaOH=5NaI+NaIO3+3H2O,依据元素化合价变化判断元素化合价升高的被氧化得到氧化产物,碘元素化合价从0价变化为+5价,升高,被氧化得到NaIO3,元素化合价降低的做氧化剂被还原得到还原产物.碘单质化合价从0价变化为-1价,化合价降低被还原,得到还原产物为NaI,所以反应①中氧化产物与还原产物的物质的量之比为1:5;
故答案为:1:5;
(2)淀粉遇碘变蓝,反应后加淀粉无现象即可说明反应结束,则判断反应①中碘是否反应完全的方法为取少量反应后的溶液于试管中,滴入几滴淀粉溶液,若溶液未变蓝,则证明碘已反应完全;反之,碘未反应完全,(或取少量反应后的溶液于试管中,滴入几滴CCl4,振荡、静置,若下层液体呈无色,证明碘已反应完全;若下层液体呈紫红色,证明碘未反应完全)
故答案为:取少量反应混合液于试管中并滴入几滴淀粉溶液,若溶液未变蓝色,证明碘已完全转化;如果溶液变蓝,则说明碘没有转化完全;
(3)向NaIO3溶液中加入铁屑的目的是还原碘酸钠得到碘化钠,反应②涉及反应为2Fe+NaIO3+3H2O=2Fe(OH)2↓+NaI,离子方程式为3Fe+IO3-+3H2O═3Fe(OH)2↓+I-,Fe(OH)2不稳定,可与空气中氧气反应而被氧化而生成Fe(OH)3,在灼烧时生成Fe2O3,则反应的总方程式为4Fe(OH)2+O2
2 Fe2O3+4H2O,
故答案为:还原碘酸钠得到碘化钠,3Fe+IO3-+3H2O═3Fe(OH)2↓+I-;
(4)NaI不稳定,易被氧化而变质,在加热浓缩溶液时应充入氮气,以隔绝空气而防止被氧气氧化,
故答案为:防止NaI被空气氧化; 低压蒸发浓缩,并充入氮气隔绝空气.
(1)反应①为碘单质和氢氧化钠溶液的反应生成碘化钠,碘酸钠和水,3I2+6NaOH=5NaI+NaIO3+3H2O,依据元素化合价变化判断元素化合价升高的被氧化得到氧化产物,碘元素化合价从0价变化为+5价,升高,被氧化得到NaIO3,元素化合价降低的做氧化剂被还原得到还原产物.碘单质化合价从0价变化为-1价,化合价降低被还原,得到还原产物为NaI,所以反应①中氧化产物与还原产物的物质的量之比为1:5;
故答案为:1:5;
(2)淀粉遇碘变蓝,反应后加淀粉无现象即可说明反应结束,则判断反应①中碘是否反应完全的方法为取少量反应后的溶液于试管中,滴入几滴淀粉溶液,若溶液未变蓝,则证明碘已反应完全;反之,碘未反应完全,(或取少量反应后的溶液于试管中,滴入几滴CCl4,振荡、静置,若下层液体呈无色,证明碘已反应完全;若下层液体呈紫红色,证明碘未反应完全)
故答案为:取少量反应混合液于试管中并滴入几滴淀粉溶液,若溶液未变蓝色,证明碘已完全转化;如果溶液变蓝,则说明碘没有转化完全;
(3)向NaIO3溶液中加入铁屑的目的是还原碘酸钠得到碘化钠,反应②涉及反应为2Fe+NaIO3+3H2O=2Fe(OH)2↓+NaI,离子方程式为3Fe+IO3-+3H2O═3Fe(OH)2↓+I-,Fe(OH)2不稳定,可与空气中氧气反应而被氧化而生成Fe(OH)3,在灼烧时生成Fe2O3,则反应的总方程式为4Fe(OH)2+O2
| ||
故答案为:还原碘酸钠得到碘化钠,3Fe+IO3-+3H2O═3Fe(OH)2↓+I-;
(4)NaI不稳定,易被氧化而变质,在加热浓缩溶液时应充入氮气,以隔绝空气而防止被氧气氧化,
故答案为:防止NaI被空气氧化; 低压蒸发浓缩,并充入氮气隔绝空气.
点评:本题考查物质制备实验,注意把握制备流程中发生的反应及操作,题目涉及氧化还原反应及碘的特性,注重基础知识的考查,题目难度不大.

练习册系列答案
相关题目
下列变化均可一步实现,其过程中没有电子转移的是( )
| A、Al→AlO2- |
| B、Fe→Fe3O4 |
| C、Ca(ClO)2→HClO |
| D、NO2→HNO3 |
高分子化合物 的单体是( )
的单体是( )
 的单体是( )
的单体是( )A、 |
B、 |
C、 和CH2═CH2 和CH2═CH2 |
D、 和CH3-CH3 和CH3-CH3 |
有关物质的分类中,说法错误的是( )
| A、KNO3属于硝酸盐 |
| B、CaO属于氧化物 |
| C、NaHCO3属于酸 |
| D、Na2CO3属于钠盐 |
下列装置能构成原电池的是( )
A、 |
B、 |
C、 |
D、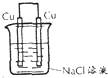 |

 (1)化学反应中均伴随着能量的变化,化学键的断裂和形成是发生能量变化的主要原因.生成物中化学键形成时会
(1)化学反应中均伴随着能量的变化,化学键的断裂和形成是发生能量变化的主要原因.生成物中化学键形成时会