题目内容
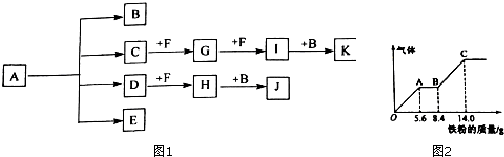
15.利用工业尾气SO2和NO可获得Na2S2O4(连二亚硫酸钠)和NH4NO3,其工艺流程图如下(Ce为铈元素):
已知:(Ⅰ)装置Ⅱ中主要反应的化学方程式为:
①2NO+2Ce(SO4)2+2H2O═Ce2(SO4)3+2HNO2+H2DO4
②2NO+6Ce(SO4)2+4H2O═3Ce2(SO4)3+2HNO3+3H2SO4
(Ⅱ)装置Ⅲ中主要反应的化学方程式为:
H2SO4+Ce2(SO4)3+2NaHSO3$\frac{\underline{\;通电\;}}{\;}$2Ce(SO4)2+Na2S2O4+2H2O
(1)写出装置I中反应的化学方程式:SO2+2NaOH=Na2SO3+H2O.
(2)用双线桥法表示装置Ⅱ中反应②的电子转移情况:
 .
.(3)根据已知信息和流程图可知可以循环使用的物质是Ce4+,该流程不但可以变废为宝,还可以减缓的环境问题是减少酸雨的形成(写一种).
(4)装置Ⅲ中氧化剂与还原剂的物质的量之比为2:1.
(5)每生产16tHN4NO3产品,至少需要标准状况下4.48×106LNH3.
分析 (1)NO与氢氧化钠溶液不反应,SO2是酸性氧化物,能与氢氧化钠溶液反应生成亚硫酸钠和水;
(2)在②2NO+6Ce(SO4)2+4H2O═3Ce2(SO4)3+2HNO3+3H2SO4中,N元素由+2升高到+5价,Ce元素由+4降低到+3价;(3)由流程图可知,装置Ⅱ加入Ce4+,装置Ⅲ产生Ce4+;根据SO2对大气的危害分析回答;
(4)该反应中,Ce2(SO4)3→Ce(SO4)2,Ce元素由+升高到+4价,Ce2(SO4)3是还原剂,NaHSO3→Na2S2O4,S元素由+4降低为+3,NaHSO3是氧化剂;
(5)根据NH3+HNO3=NH4NO3结合n=$\frac{m}{M}$、V=n•Vm计算.
解答 解:(1)NO与氢氧化钠溶液不反应,SO2是酸性氧化物,能与氢氧化钠溶液反应生成亚硫酸钠和水,化学方程式为SO2+2NaOH=Na2SO3+H2O,
故答案为:SO2+2NaOH=Na2SO3+H2O;
(2)在②2NO+6Ce(SO4)2+4H2O═3Ce2(SO4)3+2HNO3+3H2SO4中,N元素由+2升高到+5价,Ce元素由+4降低到+3价,用双线桥表示转移电子情况为 ,
,
故答案为: ;
;
(3)由流程图可知,装置Ⅱ加入Ce4+,装置Ⅲ产生Ce4+,可以循环使用;NO有毒,可对大气造成污染,而SO2对大气造成污染,可导致酸雨的形成,
故答案为:Ce4+;减少酸雨的形成;
(4)该反应中,Ce2(SO4)3→Ce(SO4)2,Ce元素由+升高到+4价,Ce2(SO4)3是还原剂,NaHSO3→Na2S2O4,S元素由+4降低为+3,NaHSO3是氧化剂,因此氧化剂与还原剂的物质的量之比为2:1,
故答案为:2:1;
(5)每生产16tHN4NO3产品,至少需要氨气的质量为xt,则
NH3+HNO3=NH4NO3
17 80
xt 16t
$\frac{17}{80}=\frac{x}{16}$,解得x=3.4,
氨气的物质的量n=$\frac{3.4×1{0}^{6}g}{17g/mol}$=2×105mol,标准状况下V=n•Vm=2×105mol×22.4L/mol=4.48×106L,
故答案为:4.48×106.
点评 本题考查了无机化工生产流程图,为高频考点,涉及氧化还原反应、计算、电化学等知识,综合性强,侧重分析、计算能力的考查,题目难度中等.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | n(CH3COOH) | B. | c(H+) | C. | c(H+)•c(OH-) | D. | $\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ |
| A. | 电镀时,待镀金属连接电源负极,发生氧化反应 | |
| B. | 工业上电解NaCl水溶液制备钠,电解熔融态Al2O3制备Al | |
| C. | 往往将铁闸门与直流电源的负极相连,这是牺牲阳极的阴极保护法 | |
| D. | 电解精炼铜时,电解液选用硫酸酸化的硫酸铜,精炼过程中,Cu2+浓度降低 |
| A. | 漂白粉、盐酸、碘酒和液氯都属于混合物 | |
| B. | 向煮沸的1 mol/L NaOH溶液中滴加FeCl3饱和溶液,可制备Fe(OH)3胶体 | |
| C. | 熔融氯化钠,盐酸和铜都能导电,所以都属于电解质 | |
| D. | 一束平行光线照射蛋白质溶液时,从侧面可以看到一束光亮的通路 |
| A. | Na2S溶液:c(Na+)>c(HS-)>c(OH-)>c(H2S) | |
| B. | Na2C2O4溶液中:c(OH-)=c(H+)+c(HC2O4-)+2c(H2C2O4)+c(C2O42-) | |
| C. | Na2CO3溶液:c(Na+)+c(H+)=2c(CO32-)+c(OH-) | |
| D. | CH3COONa和CaCl2混合溶液:c(Na+)+2c(Ca2+)=c(CH3COO-)+c(CH3COOH)+c(Cl-) |
| A. | NaB溶液的pH=8,c(Na+)-c(B-)=9.9×10-6mol•L-1 | |
| B. | pH相等的①NH4C1、②(NH4)2SO4、③NH4HSO4三种溶液中,c(NH4+)大小顺序为:①=②>③ | |
| C. | Na2CO3溶液中,2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) | |
| D. | 10mLpH=12的氢氧化钠溶液中加入pH=2的HA至pH刚好等于7,所得溶液体积V(总)≥20mL |
| A. | SO3 | B. | BaSO4 | C. | Cl2 | D. | CH3COOH |
已知:①乙烯是一种无色稍有气味气体,难溶于水,易溶于四氯化碳等有机溶剂:②SO2易溶于水,难溶于四氯化碳等有机溶剂.
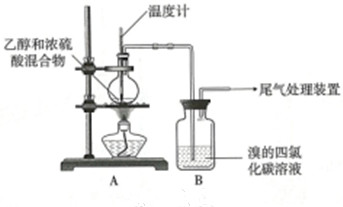
| 操作 | 现象 |
| 点燃酒精灯, 加热至170℃ | a.A中烧瓶内液体渐渐变黑 b.B内气泡连续冒出,溶液逐渐褪色 |
| … | |
| 实验完毕 | c.A中烧瓶内附着少量黑色颗粒状物,有刺激性气味逸出 |
(2)加入沸石的作用是防止瀑沸;若加热后发现未加沸石,应采取的操作是待溶液冷却后再补加.
(3)分析使B中溶液褪色的物质,甲认为是C2H4,乙认为不能排除SO2的作用.
①根据甲的观点,C2H4使B中溶液褪色的化学方程式为CH2=CH2+Br2→CH2Br-CH2Br.
②乙根据现象c认为产生了SO2,写出SO2使B中溶液褪色的离子方程式:SO2+Br2+2H2O=4H++2 Br-+SO42-.
(4)为证实各自观点,甲、乙同学重新实验,各自在A、B间增加一个装有某种试剂的洗气瓶,均观察到溴水褪色.
①根据甲的设计,洗气瓶中盛放的试剂是NaOH溶液.
②乙为进一步验证其观点,取少量反应后的B中溶液,加入少量BaCl2溶液,振荡,产生大量白色沉淀,反应的离子方程式为SO2+2H2O+Br2═4H++2Br-+SO42-、SO42-+Ba2+═BaSO4↓或SO2+2H2O+Br2+Ba2+═4H++2Br-+BaSO4↓.