题目内容
下列各组物质的性质比较中不正确的是( )
| A、热稳定性:H2S>PH3>SiH4 |
| B、原子半径:Na>Mg |
| C、碱性:NaOH>Mg(OH)2>Al(OH)3 |
| D、结合质子能力:Cl->S2- |
考点:元素周期律的作用
专题:元素周期律与元素周期表专题
分析:A、元素的非金属性越强,对应的氢化物越稳定;
B、同周期,从左向右原子半径在减小;
C、元素的金属性越强,对应的最高价氧化物的水化物的碱性越强;
D、酸性越弱,酸越难电离,对应的酸根离子越易结合氢离子;
B、同周期,从左向右原子半径在减小;
C、元素的金属性越强,对应的最高价氧化物的水化物的碱性越强;
D、酸性越弱,酸越难电离,对应的酸根离子越易结合氢离子;
解答:
解:A.非金属性:S>P>Si,元素的非金属性越强,对应的氢化物越稳定,所以热稳定性:H2S>PH3>SiH4,故A正确;
B.同周期元素从左到右原子半径逐渐减小,则原子半径:Na>Mg,故B正确;
C.金属性:Na>Mg>Al,元素的金属性越强,对应的最高价氧化物的水化物的碱性越强,则碱性:NaOH>Mg(OH)2>Al(OH)3,故C正确;
D.因为HCl酸性强于H2S,酸越弱,对应的阴离子越易结合质子,所以结合质子能力:S2->Cl-,故D错误.
故选D.
B.同周期元素从左到右原子半径逐渐减小,则原子半径:Na>Mg,故B正确;
C.金属性:Na>Mg>Al,元素的金属性越强,对应的最高价氧化物的水化物的碱性越强,则碱性:NaOH>Mg(OH)2>Al(OH)3,故C正确;
D.因为HCl酸性强于H2S,酸越弱,对应的阴离子越易结合质子,所以结合质子能力:S2->Cl-,故D错误.
故选D.
点评:本题考查较为综合,涉及元素周期律、酸性的比较,侧重于学生的分析能力的考查,选项D直接做有一定的难度,但如果考虑对应物质电离程度越大,其离子结合质子能力越小就简单了.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列各组离子在指定溶液中能大量共存的是( )
| A、能使甲基橙变红的溶液中:Na+、K+、AlO2-、SO42- | ||
B、
| ||
| C、加入Al能放出H2 的溶液中:Br-、HSO3 -、SO42-、Fe2+ | ||
| D、由水电离出的c(OH-)=10-11mol?L-1 的溶液中:Na+、K+、Cl-、NO3- |
下列说法正确的是( )
| A、2012 年环保热词“PM2.5”是指大气中直径小于或等于2.5 微米(1 微米=1×10-6 米)的颗粒,“PM2.5”与空气形成的分散系属于胶体 |
| B、石墨烯是一种从石墨材料中用“撕裂”方法剥离出的单层碳原子面材料,用这种方法从C60、金刚石等中获得“只有一层碳原子厚的碳薄片”也必将成为研究方向 |
| C、任何元素的原子都是由核外电子和核内中子、质子组成的 |
| D、分类方法、统计方法、定量研究、实验方法和模型化方法等是化学研究的常用方法 |
下列说法正确的是( )
| A、同一主族的金属元素,从上到下阳离子的氧化性逐渐增强 |
| B、最外层电子数相同的微粒,其化学性质一定相似 |
| C、同周期金属元素的氧化物对应水化物的碱性从左到右依次增强 |
| D、第ⅦA族元素从上到下,其氢化物稳定性减弱而还原性增强 |
葡萄糖燃烧的热化学反应方程式:C6H12O6(s)+6O2(g)→6CO2(g)+6H2O(l)+2870kJ,此反应说明( )
| A、自然界中的一切物质的能量均来自太阳 |
| B、人体每摄入1摩尔葡萄糖,就为人体提供2870kJ能量 |
| C、人体所需的能量均来自于葡萄糖的氧化 |
| D、1摩尔固态葡萄糖和6摩尔氧气所含能量大于6摩尔CO2和6摩尔液态水所含的总能量 |
“21金维他”中含有铁、钾、钙等多种成分,这里的铁、钾、钙是指( )
| A、单质 | B、元素 | C、分子 | D、原子 |
下列解释实验现象的反应方程式正确的是( )
| A、切开的金属Na暴露在空气中,光亮表面逐渐变暗2Na+O2═Na2O2 |
| B、向Na2CO3溶液中滴加HCl溶液,立即有气体产生CO32-+2H+═H2O+CO2↑ |
| C、Na2O2在潮湿的空气中放置一段时间,变成白色黏稠物2Na2O2+2CO2═2Na2CO3+O2 |
| D、向NaHCO3溶液中逐滴加入澄清石灰水,出现白色沉淀2HCO3-+Ca2++2OH-═CaCO3↓+CO32-+2H2O |

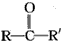 (R、R’代表烷基或H原子)发生缩合反应生成新的有机物和水.苯酚还能发生如图1反应生成有机酸酯:
(R、R’代表烷基或H原子)发生缩合反应生成新的有机物和水.苯酚还能发生如图1反应生成有机酸酯: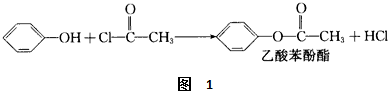
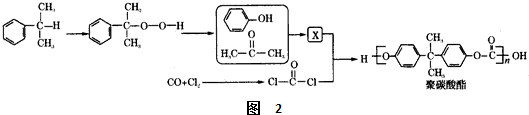
 反应合成聚碳酸酯的化学方程式
反应合成聚碳酸酯的化学方程式