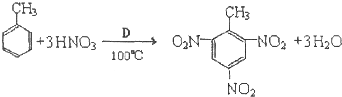
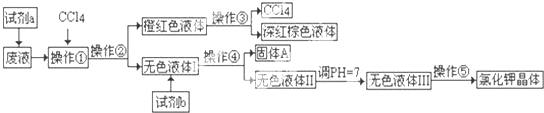
题目内容
有M、N两种溶液,各含有下列12种离子中的6种,且所含离子各不相同:Al3+、Na+、K+、Cl-、NO3-、OH-、Fe3+、Ba2+、H+、SO32-、MnO4-、AlO2-.已知每组溶液中的阳离子至少有2种,则下列说法正确的是( )
| A、若溶液M呈强酸性,则N中一定含有OH-、NO3- |
| B、若溶液N呈强酸性,则N中一定含有Al3+、可能含有Na+ |
| C、若溶液N无色,则N中一定不含有Fe3+、Cl-,且溶液M有强氧化性 |
| D、常温下,若M、N两溶液混合后pH=7,则至少生成三种沉淀 |
考点:离子共存问题
专题:
分析:两溶液所含离子各不相同,M溶液里的阳离子只有两种,由H+、Fe3+、Al3+均能与OH-反应,则M中的阳离子为K+、Na+,N中的阳离子为H+、Fe3+、Al3+,则与N中阳离子反应的阴离子应在M中,剩余的阴离子在N中,以此来解答.
解答:
解:由溶液中离子之间的反应可知,Al3+、Fe3+、H+与OH-,不能大量共存,且M溶液里的阳离子只有两种,所以Al3+、Fe3+、H+在N溶液中,OH-在M溶液中,由此知,M溶液呈碱性,N溶液呈酸性;
N溶液呈酸性,能和酸反应的离子AlO2-、SO32-不能在N溶液中,只能在M溶液中,高锰酸根离子有强氧化性,不能和氯离子、SO32-共存,所以氯离子和SO32-存在于M溶液中,M溶液里的阳离子至少有两种,Na+、K+也在M溶液中,M、N两溶液各含下列12种离子中的6种,所以NO3-在N溶液中,Ba2+与SO32-反应生成沉淀,
由以上分析知,M溶液中存在的离子为:Cl-、Na+、K+、OH-、SO32-、AlO2-;
N溶液中存在的离子为Al3+、Fe3+、Ba2+、NO3-、MnO4-、H+.
M、N可互换,
A.溶液M呈强酸性,则N中一定含有OH-,不含NO3-,故A错误;
B.溶液N呈强酸性,则N中一定含有Al3+、不含有Na+,故B错误;
C.溶液N无色,则N中一定含Cl-、Na+、K+、OH-、SO32-、AlO2-,不含有Fe3+,且溶液M含MnO4-有强氧化性,故C错误;
D.常温下,若M、N两溶液混合后pH=7,则至少生成三种沉淀,生成硫酸钡、氢氧化铁、氢氧化铝沉淀,故D正确;
故选D.
N溶液呈酸性,能和酸反应的离子AlO2-、SO32-不能在N溶液中,只能在M溶液中,高锰酸根离子有强氧化性,不能和氯离子、SO32-共存,所以氯离子和SO32-存在于M溶液中,M溶液里的阳离子至少有两种,Na+、K+也在M溶液中,M、N两溶液各含下列12种离子中的6种,所以NO3-在N溶液中,Ba2+与SO32-反应生成沉淀,
由以上分析知,M溶液中存在的离子为:Cl-、Na+、K+、OH-、SO32-、AlO2-;
N溶液中存在的离子为Al3+、Fe3+、Ba2+、NO3-、MnO4-、H+.
M、N可互换,
A.溶液M呈强酸性,则N中一定含有OH-,不含NO3-,故A错误;
B.溶液N呈强酸性,则N中一定含有Al3+、不含有Na+,故B错误;
C.溶液N无色,则N中一定含Cl-、Na+、K+、OH-、SO32-、AlO2-,不含有Fe3+,且溶液M含MnO4-有强氧化性,故C错误;
D.常温下,若M、N两溶液混合后pH=7,则至少生成三种沉淀,生成硫酸钡、氢氧化铁、氢氧化铝沉淀,故D正确;
故选D.
点评:本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重氧化还原反应、复分解反应的离子共存考查,题目难度不大.

练习册系列答案
相关题目
在强碱性溶液中能大量共存的离子组是( )
| A、Na+、NH4+、H+、NO3- |
| B、K+、Ca2+、HCO3-、NO3- |
| C、Na+、Mg2+、Cl-、NO3- |
| D、Na+、Ba2+、NO3-、Cl- |
已知I-、Fe2+、SO2、Cl-和H2O2均有还原性,它们在酸性溶液中还原性强弱顺序为Cl-<Fe2+<H2O2<I-<SO2,则下列反应不能发生的是( )
| A、H2O2+H2SO4=SO2↑+O2↑+2H2O |
| B、2Fe3++SO2+2H2O=2Fe2++SO42-+4H+ |
| C、SO2+I2+2H2O=H2SO4+2HI |
| D、Cl2+SO2+2H2O=H2SO4+2HCl |
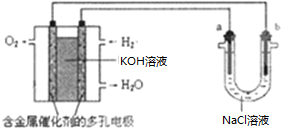
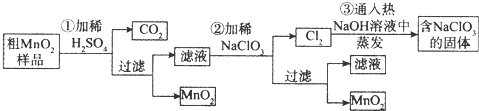
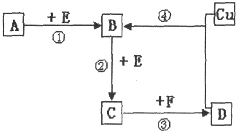 A、B、C、D、F是常见的化合物,其中F在常温下是一种无色液体,D为强酸,请根据如图转化关系(反应条件及部分产物已略去),回答下列问题:
A、B、C、D、F是常见的化合物,其中F在常温下是一种无色液体,D为强酸,请根据如图转化关系(反应条件及部分产物已略去),回答下列问题: