题目内容
若按图甲装置进行实验,图乙中x、y分别表示流入电极的电子、某产物的物质的量.若将甲装置中的溶液改为等体积、等物质的量浓度的CuSO4和NaCl溶液的混合液,电解过程中溶液的pH随时间t变化的示意图如丙所示.则下列叙述中正确的是( )
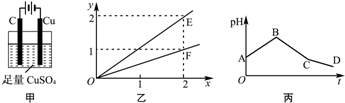

分析:电解硫酸铜溶液时,阴极发生4OH--4e-═2H2O+O2↑,阳极发生Cu2++2e-═Cu,由图象乙可知,转移电子与产物的物质的量之比,以此来分析A、B;
电解CuSO4和NaCl溶液的混合液,阴极反应先发生Cu2++2e-═Cu,后发生2H++2e-═H2↑,而阳极先发生2Cl--2e-═Cl2↑,后发生4OH--4e-═2H2O+O2↑,以此来分析B、D.
电解CuSO4和NaCl溶液的混合液,阴极反应先发生Cu2++2e-═Cu,后发生2H++2e-═H2↑,而阳极先发生2Cl--2e-═Cl2↑,后发生4OH--4e-═2H2O+O2↑,以此来分析B、D.
解答:解:电解硫酸铜溶液时,阴极发生4OH--4e-═2H2O+O2↑,阳极发生Cu2++2e-═Cu,总反应为2CuSO4+2H2O
2H2SO4+2Cu+O2↑;
电解CuSO4和NaCl溶液的混合液,阴极反应先发生Cu2++2e-═Cu,后发生2H++2e-═H2↑,而阳极先发生2Cl--2e-═Cl2↑,后发生4OH--4e-═2H2O+O2↑;
A.由图可知,E表示转移电子和生成物质的物质的量之比为1:1,而转移电子与生成Cu的物质的量之比为2:1,故A错误;
B.由2CuSO4+2H2O
2H2SO4+2Cu+O2↑~4e-可知,转移电子和生成物质的物质的量之比为1:2,即F表示反应生成H2SO4的物质的量,故B正确;
C.BC段发生4OH--4e-═2H2O+O2↑,故C错误;
D.CD段发生2H++2e-═H2↑、4OH--4e-═2H2O+O2↑,即CD段电解的物质是水,故D正确;
故选BD.
| ||
电解CuSO4和NaCl溶液的混合液,阴极反应先发生Cu2++2e-═Cu,后发生2H++2e-═H2↑,而阳极先发生2Cl--2e-═Cl2↑,后发生4OH--4e-═2H2O+O2↑;
A.由图可知,E表示转移电子和生成物质的物质的量之比为1:1,而转移电子与生成Cu的物质的量之比为2:1,故A错误;
B.由2CuSO4+2H2O
| ||
C.BC段发生4OH--4e-═2H2O+O2↑,故C错误;
D.CD段发生2H++2e-═H2↑、4OH--4e-═2H2O+O2↑,即CD段电解的物质是水,故D正确;
故选BD.
点评:本题考查电解原理,明确电解过程中离子的移动及离子的放电顺序、发生的电极反应是解答本题的关键,并注意结合图象来分析解答,题目难度中等.

练习册系列答案
相关题目


