题目内容
10.A、B两种元素的原子当它们分别获得两个电子形成惰性元素的电子层结构时,A放出的能量大于B;C、D两元素的原子,当它们分别失去一个电子也形成惰性元素的电子层结构时,吸收的能量D大于C,则A、B和C、D间分别形成离子化合物可能性最大的是( )| A. | C2A | B. | C2B | C. | D2A | D. | D2B |
分析 A、B两元素的原子分别获得两个电子形成稳定结构时,A放出的能量大于B放出的能量.说明A得电子的能量强于B,非金属性比B强;
C、D两元素的原子分别失去一个电子形成稳定结构时,D吸收的能量大于C吸收的能量.说明C失电子的能力比D高,金属性比D高,以此解答该题
解答 解:得电子形成稳定结构放出的能量越多,说明元素原子越易得电子,元素的非金属性越强,同理,失电子形成稳定结构吸收的能量越多,说明元素原子越难失电子,元素的金属性越弱,
A、B两元素的原子分别获得两个电子形成稳定结构时,A放出的能量大于B放出的能量.说明A得电子的能量强于B,非金属性比B强;
C、D两元素的原子分别失去一个电子形成稳定结构时,D吸收的能量大于C吸收的能量.说明C失电子的能力比D高,金属性比D高,
因此,A、C之间最易形成离子化合物.
故选A.
点评 本题考查原子的结构与元素周期律的关系,为高频考点,题目难度不大,注意原子得失电子与能量的大小关系和非金属性、金属性强弱的联系.

练习册系列答案
相关题目
1.化学用语是学习化学的重要工具,下列化学用语中,正确的是( )
| A. | 25℃时NH4Cl溶液的KW大于100℃时NaCl溶液的KW | |
| B. | SO2通入碘水中,反应的离子方程式为SO2+I2+2H2O=SO32-+2I-+4H+ | |
| C. | 加入铝粉能产生H2的溶液中,可能存在大量的Na+、Ba2+、NO3- | |
| D. | 100℃时,将pH=2的盐酸与pH=12的NaOH溶液等体积混合,溶液显中性 |
1.下列各组离子在指定条件的水溶液中能大量共存的是( )
| A. | 使石蕊变红色溶液:Ca2+、K+、HCO3-、Cl- | |
| B. | 强碱性的无色溶液:Na+、Ba2+、OH-、Cl- | |
| C. | PH=7的无色溶液:NH4+、Mg2+、MnO4-、HCO3- | |
| D. | 加锌能产生氢气的溶液:H+、Cu2+、CO32-、NO3- |
18.手指上有油脂(有机物)、氯化钠、水等分泌物,将按有指纹的白纸置于盛有少量单质碘的烧杯上,微热,即可显现出棕色指纹.下列碘的性质与该实验无关的是( )
| A. | 易升华 | B. | 蒸气呈紫色 | C. | 易溶于油脂 | D. | 与淀粉显蓝色 |
5.向X的溶液中加入Y试剂,产生的沉淀或气体如图所示,与所述情形相符的是( )
| A. |  向HCl和AlCl3的混合液中滴加NaOH溶液 | |
| B. |  向NaOH和Ca(OH)2的混合液中通入CO2 | |
| C. |  向NH4Al(SO4)2溶液中滴加 Ba(OH)2溶液 | |
| D. |  向NaOH和Na2CO3的混合液中滴加稀HCl溶液 |
15.从矿物学资料查得,一定条件下自然界存在如下反应:14CuSO4+5FeS2+12H2O→7Cu2S+5FeSO4+12H2SO4.下列说法正确的是( )
| A. | Cu2S既是氧化产物又是还原产物 | |
| B. | 发生反应,有10mol电子转移 | |
| C. | 产物中的SO42-有一部分是氧化产物 | |
| D. | FeS2既是氧化剂又是还原剂 |
2.关于0.1mol•L-1NaHCO3溶液,下列说法正确的是( )
| A. | 溶质水解反应:HCO3-+H2O?H3O++CO32- | |
| B. | 离子浓度关系:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(CO32-) | |
| C. | 微粒浓度关系:c(Na+)>c(HCO3-)>c(H2CO3)>c(CO32-) | |
| D. | 微粒浓度关系:c(Na+)=2[c(HCO3-)+c(CO32-)+c(H2CO3)] |
19.聚苯乙烯塑料在生产、生活中有广泛应用,其单体苯乙烯可由乙苯和二氧化碳在一定条件下发生如下反应制取: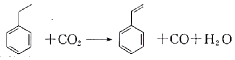
下列有关苯乙烯的说法正确的是( )

下列有关苯乙烯的说法正确的是( )
| A. | 分子中含有4个碳碳双键 | B. | 属于不含极性键的共价化合物 | ||
| C. | 分子式为C8H10 | D. | 通过加聚反应生成聚苯乙烯 |
