题目内容
13.设NA为阿伏伽德罗常数的值,下列说法正确的是( )| A. | 4.6g由NO2和N2O4组成的混合物中氧原子总数为0.2NA | |
| B. | 标准状况下,22.4L的SO3中含3NA个氧原子 | |
| C. | 100mL18.4mol/L的浓硫酸与足量的铜加热反应,转移的电子数为1.84NA | |
| D. | 密闭的容器中,催化剂作用下0.5molN2与1.5molH2反应后得到NH3分子数一定为NA |
分析 A、NO2和N2O4的最简式均为NO2;
B、标况下三氧化硫为固体;
C、铜只能与浓硫酸反应,和稀硫酸不反应;
D、合成氨的反应为可逆反应,不能进行彻底.
解答 解:A、NO2和N2O4的最简式均为NO2,故4.6g混合物中含有的NO2的物质的量为0.1mol,则含有0.2NA个氧原子,故A正确;
B、标况下三氧化硫为固体,故不能根据气体摩尔体积来计算其物质的量和含有的氧原子个数,故B错误;
C、铜只能与浓硫酸反应,和稀硫酸不反应,故浓硫酸不能反应完全,则转移的电子数小于1.84NA个,故C错误;
D、合成氨的反应为可逆反应,不能进行彻底,故得到的氨气分子个数小于NA个,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
4.除去下列混合物中的少量杂质(括号内的物质为杂质)所选试剂主要仪器及操作方法都合理的是( )
| 选项 | 样品(杂质) | 加入试剂主 | 要仪器 | 主要操作方法 |
| A | Fe2O3(Al2O3) | NaOH溶液 | 长颈漏斗 | 过滤、洗涤 |
| B | NaCl(NH4Cl) | Ca(OH)2 | 试管 | 加热 |
| C | 乙醇(水) | CaO | 蒸馏烧瓶 | 蒸馏 |
| D | NaCl溶液(Br2) | 乙醇 | 分液漏斗 | 萃取、蒸馏 |
| A. | A | B. | B | C. | C | D. | D |
1.设NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 标准状况下的22.4L辛烷完全燃烧,生成二氧化碳分子数为8NA | |
| B. | 20g重水中含有的电子数为10NA | |
| C. | 常温下,5.6g铁与足量的盐酸反应,失去的电子数为0.3NA | |
| D. | 1L 0.1mol/L NH4Cl溶液中含NH4+数为0.1NA |
8.下列有机物分离提纯的方法正确的是( )
| A. | 除去苯中少量苯酚,加入适量浓溴水,过滤 | |
| B. | 除去乙烷中的乙烯,把混合气体通入酸性高锰酸钾溶液中 | |
| C. | 除去丁醇中的乙醚,用蒸馏法 | |
| D. | 提纯蛋白质时可先加入(CH3COO)2Pb溶液,过滤后再加水重新溶解 |
18.CO分析仪以燃料电池为工作原理,用来测量汽车尾气中的CO的含量,其装置如图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动.下列说法错误的是( )
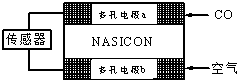

| A. | 负极的电极反应式为:CO+O2--2e-═CO2 | |
| B. | 工作时电极b作正极,O2-由电极a流向电极b | |
| C. | 工作时电子由电极a通过传感器流向电极b | |
| D. | 传感器中通过的电流越大,尾气中CO的含量越高 |
5.下列说法不正确的是( )

| A. | 苯环上有两个取代基的C9H12,其苯环上一氯代物的同分异构体(不考虑立体异构)共有10种 | |
| B. | 2,2二甲基丙醇与 2甲基丁醇互为同分异构体 | |
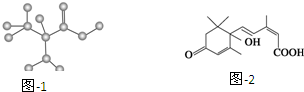
| C. | 某只含有C、H、O、N的有机物的简易球棍模型如图1所示,该有机物CH3CH2CH2NO2互为同系物 | |
| D. | S诱抗素的分子结构如图2所示,则该分子的分子式为C15H20O4 |
2.化学与生活、社会发展息息相关,下列有关说法与氧化还原反应无关的是( )
| A. | KNO3、KClO3与单质S、C2H5OH不能混搭存放在同一库房间 | |
| B. | 缺铁性补血服用补铁剂时,需与维C同时服用 | |
| C. | 铜制品、铁制品在潮湿的空气中生锈 | |
| D. | 用乙醚从黄花蒿中提取青蒿素 |
3.A、B、C、D、E五种短周期主族元素,它们的原子序数依次增大.已知:A和C、B和D分别位于同主族,且B、D质子数之和是A、C质子数之和的2倍.下列说法正确的是( )
| A. | 原子半径的大小顺序:r(B)>r(C)>r(D) | |
| B. | C的最高价氧化物对应水化物的碱性在同周期中最强 | |
| C. | E分别与A、C形成的化合物中化学键类型相同 | |
| D. | B的简单气态氢化物的热稳定性比D的弱 |