题目内容
短周期元素W、X、Y、Z的原子序数依次增大,W与Y、X与Z位于同一主族,W与X可形成共价化合物WX2,Y原子的内层电子总数是其最外层电子数的2.5倍.下列叙述中不正确的是( )
| A、WZ2分子中所有原子最外层都为8电子结构 |
| B、原子半径大小顺序为X<W<Y<Z |
| C、WX2、ZX2水溶液呈酸性,都能导致酸雨 |
| D、WX2是以极性键结合成的非极性分子 |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:短周期元素W、X、Y、Z的原子序数依次增大,Y原子的内层电子总数是其最外层电子数的2.5倍,Y有三个电子层,最外层电子数为4,故Y为硅元素;W与Y,则W为碳元素;W与X可形成共价化合物WX2,X处于第ⅥA族,X与Z分别位于同一主族,故X为氧元素,Z为硫元素,以此解答.
解答:
解:短周期元素W、X、Y、Z的原子序数依次增大,Y原子的内层电子总数是其最外层电子数的2.5倍,Y有三个电子层,最外层电子数为4,故Y为硅元素;W与Y,则W为碳元素;W与X可形成共价化合物WX2,X处于第ⅥA族,X与Z分别位于同一主族,故X为氧元素,Z为硫元素.
A.C原子最外层4个电子,S原子最外层6个电子,则CS2分子中所有原子最外层都为8电子结构,故A正确;
B.同周期原子序数越大,原子半径越小,故C>O,Si>S,电子层越多原子半径越大S>C,所以原子半径Si>S>C>O,即X<W<Z<Y,故B错误;
C.二氧化碳不能形成酸雨,可导致温室效应,故C错误;
D.CO2分子中含有C-O极性键,结构对称,正负电荷的中心重合,属于直线形非极性分子,故D正确.
故选BC.
A.C原子最外层4个电子,S原子最外层6个电子,则CS2分子中所有原子最外层都为8电子结构,故A正确;
B.同周期原子序数越大,原子半径越小,故C>O,Si>S,电子层越多原子半径越大S>C,所以原子半径Si>S>C>O,即X<W<Z<Y,故B错误;
C.二氧化碳不能形成酸雨,可导致温室效应,故C错误;
D.CO2分子中含有C-O极性键,结构对称,正负电荷的中心重合,属于直线形非极性分子,故D正确.
故选BC.
点评:本题考查位置、结构、性质,为高频考点,侧重于学生的分析能力的考查,注意把握元素的原子结构特点,熟悉元素及其化合物的性质即可解答,题目难度不大.

练习册系列答案
相关题目
以下说法正确的是( )
| A、绿色食品是指不含任何化学物质的食品 |
| B、化学反应过程中必然伴随着能量的变化 |
| C、将饱和FeCl3溶液滴入沸水中形成胶体发生的是物理变化 |
| D、纳米材料是一种称为“纳米”的新物质制成的材料 |
有关化学用语正确的是( )
| A、次氯酸钙的化学式Ca(ClO)2 | ||
| B、乙酸的结构简式C2H4O2 | ||
C、氮气的电子式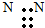 | ||
D、臭氧的化学式
|
阿伏加德罗常数约为6.02×1023mol-1,下列说法中错误的是( )
| A、16.9 g BaO2固体中阴、阳离子总数约为0.3×6.02×1023 |
| B、2.3 g 钠被O2完全氧化时,失去电子数约为0.1×6.02×1023 |
| C、0.5 mol超重水(T2O)的质子总数约为5×6.02×1023 |
| D、常温下,11.2 L甲烷与乙烯的混合物所含氢原子的数目约为2×6.02×1023 |
往溴的苯溶液中加入少量铁屑能迅速反应,其过程如下:
由上反应可知: 中的催化剂为( )
中的催化剂为( )

由上反应可知:
 中的催化剂为( )
中的催化剂为( )| A、Fe |
| B、FeBr3 |
| C、Br+ |
| D、FeBr4- |
喜树中含有一种被称为喜树碱的生物碱,这种碱的相对分子质量在300~400之间,实验分析得知其元素组成为:C占69.0%、O占18.4%,且O含量为H的4倍,其余为N,则一个喜树碱分子中含有的原子总数为( )
| A、42 | B、43 | C、44 | D、45 |
下列离子方程式正确的是( )
| A、氯气通入水中:Cl2+H2O=H++Cl-+HClO |
| B、石灰石溶于醋酸:CaCO3+2H+=Ca2++CO2↑+H2O |
| C、向Ba(OH)2 溶液中逐滴加入NaHSO4稀溶液至刚好沉淀完全:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| D、钠和冷水反应:Na+2H2O=Na++2OH-+H2↑ |
下列说法中正确的是( )
| A、“绿色食品”是指不含任何化学物质的食品 |
| B、某些植物通过叶面直接吸收空气中的氮气,然后将氮由游离态转化为化合态 |
| C、光导纤维是以单晶硅为主要原料制成的 |
| D、用热的纯碱溶液可洗去试管内壁上附着的油脂 |