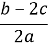题目内容
下列递变规律正确的是:
A.HClO4、H2SO4、H3PO4的酸性依次增强
B.P、S、Cl最高正价依次升高
C.HCl、HBr、HI的稳定性依次增强
D.锂、钠、钾的金属性依次增强
BD
【解析】
试题分析:A.元素的非金属性Cl>S> P。元素的非金属性越强,其最高价氧化物对应的水化物的酸性就越强。因此酸HClO4、H2SO4、H3PO4的酸性依次减弱。错误。B.P、S、Cl最外层电子数分别为5、6、7.元素的最高正价等于其元素原子的最外层电子数。所以P、S、Cl最高正价依次升高。正确。C.Cl、Br、I的非金属性逐渐减弱。元素的非金属性越强,其氢化物的稳定性就越强。所以HCl、HBr、HI的稳定性依次减弱。错误。D.锂、钠、钾是同一主族的元素,从上到下元素的原子半径逐渐增大,原子失去电子的能力逐渐增强,因此元素的金属性依次增强。正确。
考点:考查元素的构、位、性关系的知识。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列有关实验操作、现象和解释或结论都正确的是
选项 | 操作 | 现象 | 解释或结论 |
A | 过量的Fe粉中加入稀HNO3,充分反应后,滴加KSCN溶液 | 溶液呈红色 | 稀HNO3将Fe氧化为Fe3+ |
B | Al箔插入稀HNO3中 | 无现象 | Al箔表面被稀HNO3氧化, 形成致密的氧化膜 |
C | 向某溶液中滴加稀NaOH溶液,将湿润 红色石蕊试纸置于试管口 | 试纸未变蓝 | 不能确定该溶液中是否含 有NH4+ |
D | 向紫色石蕊试液中通入SO2 | 溶液褪色 | SO2有漂白性 |
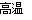 2Fe+Al2O3
2Fe+Al2O3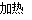 2CO
2CO  CaO+CO2↑
CaO+CO2↑ CO+H2
CO+H2
 的物质的量浓度(单位mol·L-1)为 ( )
的物质的量浓度(单位mol·L-1)为 ( ) B.
B.
 D.
D.