题目内容
18.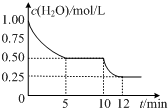 在2L密闭容器中进行反应C (s)+H2O(g)?CO(g)+H2(g)△H>0,测得c(H2O)随反应时间(t)的变化如图.下列判断正确的是( )
在2L密闭容器中进行反应C (s)+H2O(g)?CO(g)+H2(g)△H>0,测得c(H2O)随反应时间(t)的变化如图.下列判断正确的是( )| A. | 0~5min内,v (H2)=0.05mol/(L•min) | |
| B. | 5min时该反应的K值一定小于12 min时的K值 | |
| C. | 10 min时,改变的外界条件可能是减小压强 | |
| D. | 5min时该反应的v (正)大于11 min 时的v (逆) |
分析 A.根据图可知,前5min内H2O的浓度由1.00mol/L减小为0.50mol/L,根据v=$\frac{△c}{△t}$计算c(H2O),再利用速率之比等于化学计量数之比计算v(H2);
B.由图可知,10min时H2O的浓度继续减小,反应向正反应方向移动,并且10min后反应速率大于前5分钟,则不是升压就是升温,平衡常数仅与温度有关;
C.由图可知,10min时H2O的浓度继续减小,反应向正反应方向移动;
D.根据B的判断,11 min时的温度高于5min时,根据温度越高反应速率越快.
解答 解:A.根据图可知,前5min内H2O的浓度由1.00mol/L减小为0.50mol/L,根据v=$\frac{△c}{△t}$=$\frac{1mol/L-0.5mol/L}{5min}$=0.1mol/(L•min),由化学计量数之比等于反应速率之比,则v(H2)=0.1mol/(L•min),故A错误;
B.由图可知,10min时H2O的浓度继续减小,反应向正反应方向移动,该反应正反应是吸热反应,所以是升高温度,所以5 min时该反应的K值一定小于12 min时的K值,故B正确;
C.由图可知,10min时H2O的浓度继续减小,反应向正反应方向移动,该反应正反应是吸热反应,所以是升高温度,故C错误;
D.根据B的判断,11 min时的温度高于5min时,根据温度越高反应速率越快,所以5 min时该反应的v正小于11 min时的v逆,故D错误;
故选B.
点评 本题考查化学平衡图象,涉及反应速率的计算、化学平衡的影响因素、化学平衡状态本质,难度中等,注意根据浓度变化判断可能改变的条件.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.二氟甲烷是优异的环保产品,它可替代某些会破坏臭氧层的“氟利昂”产品,用作空调和冷冻库致冷剂.二氟甲烷的结构有( )
| A. | 4种 | B. | 3种 | C. | 2种 | D. | 1种 |
3.下列物质中,属于强碱的是( )
| A. | NaOH | B. | Al(OH)3 | C. | CaO | D. | NH3•H2O |
7.下列说法正确的是( )
| A. | 需要加热才能发生的反应一定是吸热反应 | |
| B. | 任何放热反应在常温下一定能发生反应 | |
| C. | 放热反应不需要加热就能发生 | |
| D. | 吸热反应在常温下也能发生 |



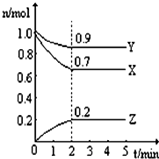 某温度时,在一个2L的密闭容器中,X、Y、Z三种气态物质的物质的量随时间的变化曲线如图所示,由图中数据分析:
某温度时,在一个2L的密闭容器中,X、Y、Z三种气态物质的物质的量随时间的变化曲线如图所示,由图中数据分析: 有A、B、C、D四种元素,A元素的原子的所有能级具有相同的电子数,由B元素形成的单质在常温常压为易挥发的液体,可从海水是提取,C及其合金是人类最早使用的金属材料.D与A位于同一主族,是构成地球上矿物质的主要元素.请回答下列问题:
有A、B、C、D四种元素,A元素的原子的所有能级具有相同的电子数,由B元素形成的单质在常温常压为易挥发的液体,可从海水是提取,C及其合金是人类最早使用的金属材料.D与A位于同一主族,是构成地球上矿物质的主要元素.请回答下列问题: