题目内容
16.(1)标准状况下,1体积水中能溶解500体积的HCl气体.若向水中通入标准状况下的44.8L HCl气体配成1L溶液,假设气体完全溶解,所得溶液密度为1.1g/cm3,则溶液中含HCl质量分数为6.6%;从该溶液中取出10mL浓盐酸溶解于水配制成250mL溶液,配制后的稀溶液中含HCl物质的量浓度为0.08mol/L.(2)将117g NaCl溶于水配制成1L溶液,)溶液中Cl-的物质的量浓度为2mol/L.配制1mol•L-1的NaCl溶液500mL,需该溶液的体积为0.25L.向该溶液中再通入一定量的HCl气体后,溶液中Cl-的物质的量浓度为3mol•L-1(假设溶液体积不变),则溶液中H+的物质的量浓度为1mol/L,通入HCl气体的体积(标准状况下)为22.4L.
分析 (1)依据m=nM计算氯化氢的质量,依据m=Vρ计算溶液的质量,依据ω=$\frac{溶质的质量}{溶液的质量}$×100%;依据溶液稀释前后所含溶质的物质的量不变计算配置后的稀溶液中含HCl物质的量浓度;
(2)根据n=$\frac{m}{M}$计算NaCl的物质的量,溶液中n(Cl-)=n(NaCl),根据c=$\frac{n}{V}$计算NaCl、Cl-的物质的量浓度;设所需氯化钠溶液的体积为VL,根据溶液稀释定律C浓V浓=C稀V稀来计算;根据电荷守恒:c(H+)+c(Na+)=c(Cl-),据此计算c(H+);根据n=cV计算溶液中H+的物质的量,而氢离子源于HCl的电离,故n(HCl)=n(H+),再根据V=nVm计算HCl的体积.
解答 解:(1)溶液的质量分数=$\frac{溶质的质量}{溶液的质量}$×100%=$\frac{2×36.5g}{1000mL×1.1g/mL}$×100%=6.6%;
设从该溶液中取出10mL浓盐酸溶解于水配置成250mL溶液,配置后的稀溶液中含HCl物质的量浓度为C,依据溶液稀释前后所含溶质的物质的量不变得:
C×250mL=2×10mL,解得C=0.08mol/L,故答案为:6.6%;0.08 mol/L;
(2)117g NaCl的物质的量=$\frac{117g}{58.5g/mol}$=2mol,溶于水配成1L溶液,故c(NaCl)=$\frac{2mol}{1L}$=2mol/L,溶液中n(Cl-)=n(NaCl)=2mol,故c(Cl-)=$\frac{2mol}{1L}$=2mol/L;
设所需氯化钠溶液的体积为VL,根据溶液稀释定律C浓V浓=C稀V稀可知:2mol/L×VL=1mol/L×0.5L,解得V=0.25L;
根据电荷守恒:c(H+)+c(Na+)=c(Cl-),故c(H+)=3mol/L-2mol/L=1mol/L,而氢离子源于HCl的电离,故n(HCl)=n(H+)=1L×1mol/L=1mol,故V(HCl)=1mol×22.4L/mol=22.4L.
故答案为:2mol/L;0.25L;1mol/L;22.4L.
点评 本题考查物质的量浓度计算,难度不大,注意对公式的理解与灵活应用,(2)题中应注意电解质混合溶液中离子浓度计算常用电荷守恒解答.

 全能测控期末小状元系列答案
全能测控期末小状元系列答案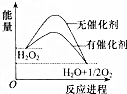 已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如图所示.下列说法正确的是( )
已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如图所示.下列说法正确的是( )| A. | 反应物的总能量高于生成物的总能量 | |
| B. | 加入催化剂,可提高H2O2的平衡转化率 | |
| C. | H2O2分解的热化学方程式:H2O2=H2O+O2;△H=-Q1 kJ•mol-1 | |
| D. | 加入催化剂,减小了反应的热效应 |
| A. | 标准状况下,铝跟氢氧化钠溶液反应生成1mol氢气时,转移的电子数为2NA | |
| B. | 7 g CnH2n中含有的氢原子数目为NA | |
| C. | 任何气体单质在标况下体积若为22.4L,则含有2NA个原子 | |
| D. | 1mol Na2O2与水反应转移的电子数约为1.204×1024个 |
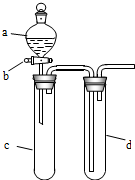 某兴趣小组设计出如图所示装置来改进教材中“铜与硝酸反应”实验,以探究化学实验的绿色化.
某兴趣小组设计出如图所示装置来改进教材中“铜与硝酸反应”实验,以探究化学实验的绿色化.(1)实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,加热c,其目的是检查装置气密性.
(2)下表是制取硝酸铜的三种方案,能体现绿色化学理念的最佳方案是丙.
| 方案 | 反应物 |
| 甲 | Cu、浓HNO3 |
| 乙 | Cu、稀HNO3 |
| 丙 | Cu、O2、稀HNO3 |
| A. | KI溶液在空气久置变黄:4I-+O2+4H+=2I2+2H2O | |
| B. | 用稀盐酸除去久存石灰水的烧杯内壁上的固体:2H++Ca(OH)2=Ca2++2H2O | |
| C. | 用酸性KMnO4溶液除去CO2中SO2:3SO2+2MnO4-+4H+=3SO42-+2MnO2↓+H2O | |
| D. | 用足量饱和Na2CO3溶液吸收制备的乙酸乙酯:CO32-+CH3COOH=HCO3-+CH3COO- |
