题目内容
下列反应属于放热反应的是( )
| A、氢氧化钡晶体和氯化铵晶体的反应 |
B、能量变化如图所示的反应 |
| C、化学键断裂吸收的热量比化学键生成放出的热量多的反应 |
| D、燃烧反应和中和反应 |
考点:吸热反应和放热反应
专题:化学反应中的能量变化
分析:A.铵盐和碱的反应是吸热反应;
B.放热反应中反应物的总能量大于生成物的总能量;
C.断键吸收能量,成键放出能量;
D.中和反应是放热反应.
B.放热反应中反应物的总能量大于生成物的总能量;
C.断键吸收能量,成键放出能量;
D.中和反应是放热反应.
解答:
解:A.氢氧化钡晶体和氯化铵晶体的反应是吸热反应,故A错误;
B.反应物的总能量小于生成物的总能量,为吸热反应,故B错误;
C.化学键断裂吸收的热量比化学键生成放出的热量多的反应为吸热反应,故C错误;
D.燃烧反应和中和反应是放热反应,故D正确.
故选D.
B.反应物的总能量小于生成物的总能量,为吸热反应,故B错误;
C.化学键断裂吸收的热量比化学键生成放出的热量多的反应为吸热反应,故C错误;
D.燃烧反应和中和反应是放热反应,故D正确.
故选D.
点评:本题考查化学反应中能量变化,题目难度不大,掌握常见的放热反应和吸热反应是解题的关键.

练习册系列答案
 黄冈创优卷系列答案
黄冈创优卷系列答案
相关题目
下列化学用语说法正确的是( )
A、甲基的电子式: | ||
B、乙烯的比例模型: | ||
C、质子数为53,中子数为78的碘原子:
| ||
| D、次氯酸的结构式:H─O─Cl |
下列说法不正确的是( )
| A、离子交换膜在工业生产中广泛应用,如氯碱工业使用了阴离子交换膜 | ||
| B、人造纤维可利用竹子、棉花、麻类的纤维材料制成,而合成纤维是利用自然界的非纤维材料(如石油、煤)通过化学合成方法得到 | ||
| C、有机玻璃是以有机物A(甲基丙烯酸甲酯)为单体,通过加聚反应得到,合成A的一种途经是: CH3C≡CH+CO+CH3OH
 ,其过程符合绿色化学的原则 ,其过程符合绿色化学的原则 | ||
| D、温室效应导致海水的酸度增加,珊瑚、贝壳类等生物的生存将会受到威胁 |
NA为阿伏加德罗常数,下列说法正确的是( )
| A、标准状况下,11.2L的戊烷所含的分子数为0.5NA |
| B、28g乙烯所含共用电子对数目为4NA |
| C、1mol甲基的电子数目为7NA |
| D、现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为3NA |
下列有关晶体的说法中一定正确的是( )
①依据构成粒子的堆积方式可将晶体分为金属晶体、离子晶体、分子晶体、原子晶体;
②由原子直接构成的晶体就是原子晶体;
③分子晶体的堆积均采取分子密堆积;
④NaF、MgF2、SiF4三种晶体的熔点依次升高;
⑤金属键只存在于金属晶体中;
⑥离子键只存在于离子晶体中;
⑦H2O的性质非常稳定,原因在于分子之间存在氢键;
⑧SO2和SiO2晶体在熔化时破坏的作用力相同.
①依据构成粒子的堆积方式可将晶体分为金属晶体、离子晶体、分子晶体、原子晶体;
②由原子直接构成的晶体就是原子晶体;
③分子晶体的堆积均采取分子密堆积;
④NaF、MgF2、SiF4三种晶体的熔点依次升高;
⑤金属键只存在于金属晶体中;
⑥离子键只存在于离子晶体中;
⑦H2O的性质非常稳定,原因在于分子之间存在氢键;
⑧SO2和SiO2晶体在熔化时破坏的作用力相同.
| A、①⑤⑥⑦ | B、只有⑥ |
| C、②③⑤⑥ | D、①②⑤⑧ |
一定温度下,可逆反应H2(g)+I2(g)?2HI(g)达到限度的标志是( )
| A、H2,I2,HI三种物质的浓度一定相等 |
| B、H2,I2全部反应生成了HI |
| C、H2,I2,HI三种物质的浓度保持不变 |
| D、反应中正反应速率逐渐减小,最后减小为零 |
下列有关化学用语使用正确的是( )
A、硫原子的原子结构示意图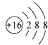 | ||
B、NH4Cl的电子式: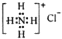 | ||
C、原子核内有10个中子的氧原子:
| ||
| D、基态铜原子的电子排布式为:1s22s22p63s23p63d94s2 |



