题目内容
20.填写下列空白:(1)分散系包括溶液、胶体、浊液,胶体与溶液、浊液的本质区是分散质粒子直径大小.
(2)Na2FeO4是一种高效多功能水处理剂,其中铁元素化合价为+6价,可以用NaClO在碱性溶液中与Fe(OH)3反应生成,写出生成Na2FeO4的离子方程式:3ClO-+4OH-+2Fe(OH)3=2FeO42-+3Cl-+5H2O.该反应中有1mol Na2FeO4转移的电子数为3NA.
(3)9.5g某二价金属的氯化物ACl2中含有0.2mol Cl-离子,A的相对原子质量是24.
(4)Fe2(SO4)3是工业上常用的净水剂,净水的原理是Fe3++3H2O?Fe(OH)3+3H+ (用离子方程式表示).在400mLFe2(SO4)3溶液中含Fe3+ 11.2g,取该溶液100mL,加水稀释至400mL,则此稀溶液中Fe3+的物质的量浓度为0.125 mol/L.
分析 (1)根据三类分散系的本质差异是分散质粒子的大小回答;
(2)ClO-在碱性溶液中将Fe(OH)3氧化生成FeO42-,ClO-被还原为Cl-,据此写出离子方程式;该反应中有1mol Na2FeO4生成时转移的电子数根据化合价来分析;
(3)先根据化合物与氯离子间的关系计算氯化物的物质的量,根据M=计算其摩尔质量,摩尔质量在数值上等于其相对分子质量,从而确定该金属的相对原子质量;
(4)Fe2(SO4)3中Fe3+发生水解生成氢氧化铁胶体具有吸附作用;在400mLFe2(SO4)3溶液中含Fe3+ 11.2g,取该溶液100mL,故含Fe3+为2.8g,求出Fe3+的物质的量,然后根据溶液体积增大到原来的4倍,则Fe3+的浓度将为原来的四分之一,据此计算.
解答 解:(1)当分散剂是水或其它溶液时,根据分散质粒子直径大小来分类,把分散系划分为:溶液(小于1nm)、胶体(1nm~100nm)、浊液(大于100nm),所以,溶液、胶体和浊液这三种分散系的本质的区别在于分散质粒子直径大小,故答案为:分散质粒子直径大小;
(2)ClO-在碱性溶液中将Fe(OH)3氧化生成FeO42-,ClO-被还原为Cl-,根据得失电子数守恒配平得离子方程式为:3ClO-+4OH-+2Fe(OH)3=2FeO42-+3Cl-+5H2O;该反应中有1mol Na2FeO4生成时,铁元素的化合价由+3价变为+6价,故转移3mol电子即3NA个,故答案为:3ClO-+4OH-+2Fe(OH)3=2FeO42-+3Cl-+5H2O;3NA;(3)某二价金属的氯化物中氯化物的物质的量与氯离子的物质的量之比为1:2,氯离子的物质的量为0.20mol,所以氯化物的物质的量是0.10mol,M=$\frac{m}{n}$=95g•mol-1;摩尔质量在数值上等于其相对分子质量,所以其相对分子质量为95,其相对分子质量=其相对原子质量+35.5×2=95,所以该金属元素的相对原子质量为24,故答案为:24;
(4)Fe2(SO4)3中Fe3+发生水解生成氢氧化铁胶体具有吸附作用,原理为:Fe3++3H2O?Fe(OH)3+3H+;在400mLFe2(SO4)3溶液中含Fe3+ 11.2g,取该溶液100mL,故含Fe3+为2.8g,Fe3+的物质的量n=$\frac{2.8g}{56g/mol}$=0.05mol,物质的量浓度c=$\frac{0.05mol}{0.1L}$=0.5mol/L,而溶液体积增大到原来的4倍,则Fe3+的浓度将为原来的四分之一,故稀释后溶液中Fe3+的浓度为0.125mol/L,故答案为:Fe3++3H2O?Fe(OH)3+3H+;0.125mol/L.
点评 本题考查了氧化还原反应的书写和分散质的本质区别和物质的量浓度的有关计算,难度不大,但综合性较强,注意基础的掌握.

 轻松暑假总复习系列答案
轻松暑假总复习系列答案| A. | 0.5 摩尔 | B. | 2 摩尔 | C. | 2.5 摩尔 | D. | 4 摩尔 |
| A. | 将CO2通入BaCl2溶液中至饱和,无沉淀产生;再通入SO2,产生沉淀 | |
| B. | 除去FeCl2中少量的FeBr2,加入适量氯水,再加四氯化碳萃取分液 | |
| C. | 在稀硫酸中加入铜粉,铜粉不溶解;再加入KNO3固体,铜粉仍不溶解 | |
| D. | 向AlCl3溶液中滴加1mol/L NaOH溶液10ml,产生白色沉淀;再加入1mol/L NaHSO4溶液10ml,沉淀恰好消失 |
①苯燃烧时发生明亮并带有浓烟的火焰
②苯在特定条件下能与氢气发生加成反应
③苯不与酸性高锰酸钾溶液或溴水发生反应
④苯分子具有平面正六边形结构,其中6个碳原子之间的键完全相同.
| A. | ①② | B. | ②③ | C. | ③④ | D. | ① |
| A. | NaHA溶液的pH一定大于7 | |
| B. | 在Na2A,NaHA两种溶液中,离子种类相同 | |
| C. | 在Na2A,NaHA两种溶液中都有c(OH-)+c(A2-)=c(H2A)+c(H+) | |
| D. | 在溶质的物质的量相等的Na2A,NaHA两种溶液中,阴离子总数相等 |
| A. | 当溶液中c(H+)>10-7 mol•L-1时,其pH<7,溶液呈现酸性 | |
| B. | 当溶液中c(H+)>10-7 mol•L-1时,其pH>7,溶液呈现碱性 | |
| C. | 当溶液中c(H+)=c(OH-)>10-7 mol•L-1时,其pH<7,溶液呈现中性 | |
| D. | 当溶液中c(H+)=c(OH-)>10-7 mol•L-1时,其pH<7,溶液呈现酸性 |
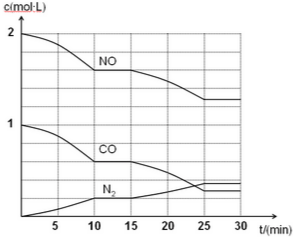
 实验室需要0.80mol/L NaOH溶液475mL和0.40mol/L硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题:
实验室需要0.80mol/L NaOH溶液475mL和0.40mol/L硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题: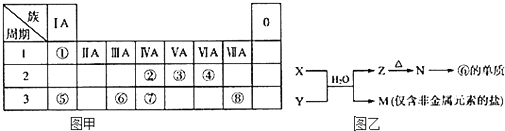
 .
.