题目内容
根据下列各题所给出的数据,可分别求出其“w%(溶质的质量分数)或c(溶质的物质的量浓度)”,试判断并求解:
(1)设NA表示阿伏加德罗常数的数值,若某NaOH溶液VL含有n个OH-,则可求出此溶液的 为 .(第一个空用符号表示,第二个空用式子表示,下同).
(2)已知某NaOH溶液中Na+与H2O的个数比为1:a,则可求出此溶液的 为 .
(3)已知标准状况下1体积水能溶解500体积的氯化氢,则可求出标准状况下氯化氢饱和溶液的 为 .(不用计算结果,列出表达式即可)
(4)已知将100mL NaHCO3的水溶液加热蒸干之后并充分灼烧,可得到白色固体bg,则可求出原NaHCO3 溶液的 为 .
(1)设NA表示阿伏加德罗常数的数值,若某NaOH溶液VL含有n个OH-,则可求出此溶液的
(2)已知某NaOH溶液中Na+与H2O的个数比为1:a,则可求出此溶液的
(3)已知标准状况下1体积水能溶解500体积的氯化氢,则可求出标准状况下氯化氢饱和溶液的
(4)已知将100mL NaHCO3的水溶液加热蒸干之后并充分灼烧,可得到白色固体bg,则可求出原NaHCO3 溶液的
考点:溶液中溶质的质量分数及相关计算,物质的量浓度的相关计算
专题:
分析:(1)根据n=
计算氢氧根离子物质的量,氢氧化钠物质的量等于氢氧根离子物质的量,再根据c=
计算氢氧化钠的物质的量浓度,溶液密度未知,不能计算溶液质量分数;
(2)根据钠离子和水分子个数之比可以计算氢氧化钠和水的质量之比,从而得出溶液的质量分数;
(3)设标准状况下1L水能溶解500L的氯化氢,根据m=ρV计算水的质量,根据n=
计算HCl物质的量,根据m=nM计算HCl质量,进而计算溶液质量,可以计算溶液质量分数;
(4)蒸干灼烧得到bg为碳酸钠质量,根据n=
计算碳酸钠物质的量,根据方程式计算碳酸氢钠的物质的量,根据c=
计算溶液物质的量浓度,溶液密度未知,不能计算溶液质量分数.
| N |
| NA |
| n |
| V |
(2)根据钠离子和水分子个数之比可以计算氢氧化钠和水的质量之比,从而得出溶液的质量分数;
(3)设标准状况下1L水能溶解500L的氯化氢,根据m=ρV计算水的质量,根据n=
| V |
| Vm |
(4)蒸干灼烧得到bg为碳酸钠质量,根据n=
| m |
| M |
| n |
| V |
解答:
解:(1)若某氢氧化钠溶液V L中含有n个OH-,则n(NaOH)=n(OH-)=
=
mol,溶液的体积为VL,因为不知溶液的密度,所以只能计算出溶质的物质的量浓度,c=
=
mol/L,
故答案为:物质的量浓度;
mol/L;
(2)氢氧化钠溶液中Na+与H2O的个数之比为1:a,结合原子守恒知,NaOH与H2O的物质的量之比为1:a,
则氢氧化钠和水的质量之比=(40g/mol×1):(18g/mol×)=20:9a,
所以可求溶质的质量分数,w=
×100%=
%,
故答案为:溶质的质量分数;
%;
(3)标准状况下1体积水能溶解500体积的氯化氢,假设水的体积是1L,氯化氢的体积是500L,水的质量是1000g,氯化氢的质量=
×36.5g/mol=,溶质和溶剂的质量都已知,所以能计算溶液的质量分数,质量分数=
×100%,
故答案为:质量分数;
×100%;
(4)蒸干灼烧得到bg为碳酸钠质量,碳酸钠物质的量为
mol,根据2NaHCO3
Na2CO3+CO2↑+H2O可知,碳酸氢钠的物质的量为
mol×2=
mol,溶液物质的量浓度为
=
mol/L,溶液密度未知,不能计算溶液质量分数,
故答案为:物质的量浓度;
mol/L.
| n |
| NAmol-1 |
| n |
| NA |
| ||
| VL |
| n |
| VNA |
故答案为:物质的量浓度;
| n |
| VNA |
(2)氢氧化钠溶液中Na+与H2O的个数之比为1:a,结合原子守恒知,NaOH与H2O的物质的量之比为1:a,
则氢氧化钠和水的质量之比=(40g/mol×1):(18g/mol×)=20:9a,
所以可求溶质的质量分数,w=
| 20 |
| 20+9a |
| 2000 |
| 20+9a |
故答案为:溶质的质量分数;
| 2000 |
| 20+9a |
(3)标准状况下1体积水能溶解500体积的氯化氢,假设水的体积是1L,氯化氢的体积是500L,水的质量是1000g,氯化氢的质量=
| 500L |
| 22.4L/mol |
| ||
1000+
|
故答案为:质量分数;
| ||
1000+
|
(4)蒸干灼烧得到bg为碳酸钠质量,碳酸钠物质的量为
| b |
| 106 |
| ||
| b |
| 106 |
| b |
| 53 |
| ||
| 0.1L |
| 10b |
| 53 |
故答案为:物质的量浓度;
| 10b |
| 53 |
点评:本题考查溶液浓度有关计算,涉及物质的量浓度、质量分数的有关计算,属于开放性题目,侧重对公式的理解与应用,难度中等.

练习册系列答案
相关题目
下列溶剂能用来萃取溴水中的溴的是( )
| A、直馏汽油 | B、裂化汽油 |
| C、环己烯 | D、酒精 |
把Na投入CuSO4溶液中可能出现的现象是( )
①生成红色的物质 ②有气体生成 ③熔成小球 ④生成蓝色沉淀.
①生成红色的物质 ②有气体生成 ③熔成小球 ④生成蓝色沉淀.
| A、①③④ | B、②③④ |
| C、①④ | D、①③④ |
下列反应的化学方程式或离子方程式表示正确的是( )
A、乙酸与乙醇的反应CH3COOH+CH3CH218OH
| ||||
| B、苯酚钠溶液和少量CO2反应:2C6H5O-+CO2+H2O=2C6H5OH+CO32- | ||||
| C、用醋酸去除水垢:CaCO3+2H+=Ca2++CO2↑+H2O | ||||
D、用银氨溶液检验乙醛的醛基:CH3CHO+2Ag(NH4)2OH
|
X、Y、Z是3种短周期元素,其中X、Y位于同一主族,Y、Z处于同一周期.X原子的最外层电子数是其电子层数的3倍.Z原子的核外电子数比Y原子少1.下列说法正确的是( )
| A、3种元素的气态氢化物中,Z的气态氢化物最稳定 |
| B、Y元素最高价氧化物对应水化物的化学式可表示为H3YO4 |
| C、元素非金属性由弱到强的顺序为Z<Y<X |
| D、原子半径由大到小的顺序为X>Y>Z |
38.4mgCu跟适量的浓HNO3反应,Cu全部作用后,共收集到22.4mL(标况)气体,反应消耗的硝酸的物质的量可能是( )
| A、1.0×10-3 mol |
| B、1.6×10-3 mol |
| C、2.2×10-3 mol |
| D、2.4×10-3 mol |
根据图式,下列热化学方程式书写正确的是( )
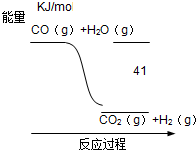

| A、CO+H2O═CO2+H2 △H=-41 KJ/mol |
| B、CO(g)+H2O(g)═CO2(g)+H2(g)△H=+41 KJ/mol |
| C、CO2(g)+H2(g)═CO(g)+H2O(g)△H=+41 KJ/mol |
| D、CO2(g)+H2(g)═CO(g)+H2O(g)△H=-41 KJ/mol |