题目内容
烧过菜的铁锅未及时洗涤(残液中含有食盐等),第二天便出现红棕色锈斑,下列反应中不属于上述整个过程中可能发生的变化的是( )
| A、2H2O+O2+4e→4OH- |
| B、Fe2++2OH-→Fe(OH)2↓ |
| C、Fe-3e→Fe3+ |
| D、4Fe(OH)2+O2+2H2O→4Fe(OH)3↓ |
考点:金属的电化学腐蚀与防护
专题:电化学专题
分析:中性条件下,钢铁发生吸氧腐蚀,C、Fe和电解质溶液构成原电池,Fe易失电子作负极、C作正极,负极反应式为Fe-2e-═Fe2+,正极反应式为2H2O+O2+4e-═4OH-,亚铁离子和氢氧根离子发生反应,亚铁离子不稳定易被氧化,据此分析解答.
解答:
解:A.中性条件下,钢铁发生吸氧腐蚀,C、Fe和电解质溶液构成原电池,Fe易失电子作负极、C作正极,正极反应式为2H2O+O2+4e-═4OH-,故A正确;
B.亚铁离子和氢氧根离子发生反应生成氢氧化亚铁,反应式为Fe2++2OH-═Fe(OH)2,故B错误;
C.负极上铁失电子生成亚铁离子,电极反应式为Fe-2e-═Fe2+,故C正确;
D.氢氧化亚铁不稳定,易被氧气氧化生成红褐色氢氧化铁,反应式为4Fe(OH)2+O2+2H2O═4Fe(OH)3,氢氧化铁失去部分水生成带结晶水的氧化铁,即铁锈,故D正确;
故选C.
B.亚铁离子和氢氧根离子发生反应生成氢氧化亚铁,反应式为Fe2++2OH-═Fe(OH)2,故B错误;
C.负极上铁失电子生成亚铁离子,电极反应式为Fe-2e-═Fe2+,故C正确;
D.氢氧化亚铁不稳定,易被氧气氧化生成红褐色氢氧化铁,反应式为4Fe(OH)2+O2+2H2O═4Fe(OH)3,氢氧化铁失去部分水生成带结晶水的氧化铁,即铁锈,故D正确;
故选C.
点评:本题考查金属腐蚀与防护,明确钢铁发生析氢腐蚀和吸氧腐蚀条件是解本题关键,注意二者区别,能正确分析各个过程发生的反应,无论发生析氢腐蚀还是吸氧腐蚀负极上都生成亚铁离子,为易错点.

练习册系列答案
 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案
相关题目
化学是一门以实验为基础的学科,化学实验是化学学习的重要内容.根据你掌握的知识判断,下列实验操作的描述中,正确的是 ( )
| A、从试剂瓶中取出的任何药品,若有剩余不能再放回原试剂瓶 |
| B、用稀盐酸洗涤盛放过石灰水的试剂瓶 |
| C、配制H2SO4溶液时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸 |
| D、各放一张质量相同的滤纸于天平的两托盘上,将NaOH固体放在左盘纸上称量 |
| E、Na2CO3溶液不能保存在带有玻璃塞的试剂瓶中 |
| F、将用水润湿的pH试纸浸入稀盐酸中,测定溶液的pH. |
下列叙述正确的是( )
| A、固体氯化钠不导电,所以氯化钠不是电解质 |
| B、氯化氢水溶液能导电,所以氯化氢是电解质 |
| C、CO2溶于水能导电,所以 CO2是电解质 |
| D、铜丝能导电,所以铜是电解质 |
对下列事实的解释错误的是( )
| A、用氢氟酸雕刻玻璃,是由于氢氟酸能与二氧化硅反应 |
| B、用75%的乙醇溶液进行消毒,是由于乙醇能使蛋白质变性 |
| C、用铁制容器储运浓硫酸或浓硝酸,是由于铁与浓硫酸或浓硝酸不反应 |
| D、向Na2O2与水完全反应后的溶液中加MnO2产生O2,可能该溶液中含H2O2 |
下列关于胶体的叙述不正确的是( )
| A、胶体区别于其他分散系的本质特征是分散质的微粒直径在10-9m~10-7m之间 |
| B、胶体是纯净物 |
| C、光线透过胶体时,胶体中可发生丁达尔效应 |
| D、Fe(OH)3胶体能吸附水中悬浮的固体颗粒并沉降,达到净水目的 |
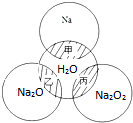 如图所示,两圆圈相交的阴影部分甲、乙、丙表示圆圈内物质相互发生的反应,钠及其氧化物的物质的量均为0.1mol,水的质量为100g.下列说法正确的是( )
如图所示,两圆圈相交的阴影部分甲、乙、丙表示圆圈内物质相互发生的反应,钠及其氧化物的物质的量均为0.1mol,水的质量为100g.下列说法正确的是( )| A、甲、乙、丙都属于氧化还原反应 |
| B、丙反应中的氧化剂是Na2O2,还原剂时H2O |
| C、丙反应中消耗1molNa2O2,则转移1mol电子 |
| D、若甲、乙、丙反应后所得溶液的质量分数分别为w1、w2、w3,则:2w1=w2=w3 |
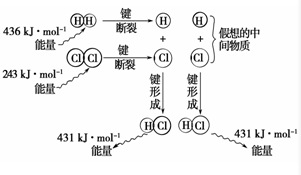 实验测得1mol H2与1mol Cl2反应生成2mol HCl时,放出184.6kJ的热量,其理论分析数据与实验数据略有差异,如图表示上述反应能量变化的理论分析示意图:
实验测得1mol H2与1mol Cl2反应生成2mol HCl时,放出184.6kJ的热量,其理论分析数据与实验数据略有差异,如图表示上述反应能量变化的理论分析示意图: