题目内容
18.红磷的化学式为P,白磷的化学式为P4,已知:P4(s)+5O2(g)→P4O10(s)+3093.2kJ4P(s)+5O2(g)→P4O10(s)+2954.0kJ,下列结论正确的是( )| A. | 白磷转化为红磷是吸热反应 | B. | 白磷比红磷稳定 | ||
| C. | 红磷转化为白磷为吸热反应 | D. | 红磷比白磷稳定 |
分析 根据已知的热化学反应方程式,利用盖斯定律来得到红磷转化为白磷的热化学反应方程式,能量的低的物质稳定,以此来解答.
解答 解:P4(s、白磷)+5O2(g)=P4O10(s);△H=-3093.2KJ•mol-1 ①
4P(s、红磷)+5O2(g)=P4O10(s);△H=-2954.0KJ•mol-1 ②
根据盖斯定律,①-②即得白磷转化为红磷的热化学方程式:P4(s、白磷)=4P(s、红磷)△H=-139.2KJ/mol,
白磷转化为红磷是放热反应,红磷转化为白磷为吸热反应,P(s、红磷)能量高稳定,
故选CD.
点评 本题考查化学反应中的能量变化及物质的稳定性,明确信息的应用得出红磷与白磷转化的热化学反应是解答本题的关键,题目难度不大.

练习册系列答案
相关题目
9.下列实验,现象和结论都正确的是( )
| 实验 | 现象 | 结论 | |
| A | Ba(NO3)2溶液中通入SO2 | 出现白色沉淀 | 有BaSO3生成 |
| B | 测定等物质的量浓度的Na2CO3和CH3COON溶液的pH | pH(Na2CO3)>pH(CH3COONa) | 不能证明碳酸和醋酸的酸性强弱 |
| C | 滴加少量乙醛于溴水中 | 溴水褪色 | 醛基和溴发生加成反应 |
| D | 在恒定温度和体积的密闭容器中,已经建立平衡N2O4(g)?2NO2(g),若加入一定量的N2O4 | 混合气体的颜色加深 | 平衡正向移动,NO2的体积分数增大 |
| A. | A | B. | B | C. | C | D. | D |
6.已知某可逆反应,x A(g)?y B(g),平衡时测得A的浓度为0.5mol/L,保持温度不变,将容器体积扩大到原来的两倍,再达到平衡时,测得A的浓度为0.3mol/L.下列判断正确的是( )
| A. | x<y | |
| B. | 平衡向正反应方向进行 | |
| C. | B的体积分数降低 | |
| D. | 缩小体积、增大压强,A的体积分数增大 |
13.除去下列括号内的杂质,所用试剂正确的是( )
| 选项 | 需除杂的物质 | 试剂 |
| A | Fe(Al) | NaOH溶液 |
| B | CO2(HCl) | NaOH溶液 |
| C | NaCl(Na2CO3) | 稀硫酸 |
| D | NH3(H2O) | 浓硫酸 |
| A. | A | B. | B | C. | C | D. | D |
10.下列有关化学实验叙述正确的是( )
| A. | 容量瓶、分液漏斗使用前都必须检查是否漏水 | |
| B. | 用98%的浓硫酸配制100 g 10%的稀硫酸时,除使用量筒外还需用到容量瓶 | |
| C. | 在钠跟水反应的实验中,切下绿豆粒大小的钠投入水中进行实验,剩余的钠块丢弃到废料桶中 | |
| D. | 配制一定物质的量浓度溶液时,用量筒量取浓溶液的体积时仰视读数,所配溶液的浓度偏低 |
7.某粉末状样品由铁、铝、铜三种金属组成,加入过量稀硫酸充分反应,过滤后向滤液中加入过量烧碱溶液,再过滤,滤液中存在的离子有( )
| A. | AIO2- | B. | Fe2+ | C. | Fe3+ | D. | Al3+ |
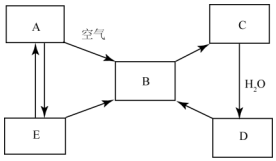 如图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去).化合物B在常温常压下为气体,B气体具有漂白性,可用于漂白纸张、草编织品等,且B和C的相对分子质量之比为4:5,化合物D是重要的工业原料,E是具有臭鸡蛋气味的气体.
如图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去).化合物B在常温常压下为气体,B气体具有漂白性,可用于漂白纸张、草编织品等,且B和C的相对分子质量之比为4:5,化合物D是重要的工业原料,E是具有臭鸡蛋气味的气体.