题目内容
有一瓶无色溶液,其中可能含有NH4+、K+、Mg2+、Ba2+、Al3+、Fe3+、I-、Cl-、NO3-、CO32-、SO42-,取该溶液进行以下实验:
(1)该溶液可使pH试纸呈现红色;
(2)取溶液少量加新制氯水及CCl4振荡,可见CCl4层呈现紫色;
(3)取溶液少量加氯化钡溶液,有白色沉淀生成,加入HNO3后沉淀不溶解;
(4)取实验(3)之上层清液,加入硝酸银溶液有白色沉淀,加入HNO3后沉淀不溶解;
(5)取原溶液少量加入NaOH溶液呈碱性,在此过程中有白色沉淀生成,而后又逐渐消失,将此溶液加热,有无色气体放出,该气体能使润湿的红色石蕊试纸变蓝.根据上述实验事实,溶液中肯定存在的离子有 ,肯定不存在的离子有 ,不能确定是否存在的离子有 .
(1)该溶液可使pH试纸呈现红色;
(2)取溶液少量加新制氯水及CCl4振荡,可见CCl4层呈现紫色;
(3)取溶液少量加氯化钡溶液,有白色沉淀生成,加入HNO3后沉淀不溶解;
(4)取实验(3)之上层清液,加入硝酸银溶液有白色沉淀,加入HNO3后沉淀不溶解;
(5)取原溶液少量加入NaOH溶液呈碱性,在此过程中有白色沉淀生成,而后又逐渐消失,将此溶液加热,有无色气体放出,该气体能使润湿的红色石蕊试纸变蓝.根据上述实验事实,溶液中肯定存在的离子有
考点:常见阳离子的检验,常见阴离子的检验
专题:物质检验鉴别题
分析:①该溶液可使pH试纸呈现红色是酸性溶液;
②溶液少量加新制氯水及CCl4振荡,碘单质能使CCl4层呈紫色;
③加入氯化钡溶液,有白色沉淀生成,加入HNO3后沉淀不溶解,则该白色沉淀是硫酸钡;
④溶液中加入硝酸银溶液有白色沉淀,加入HNO3后沉淀不溶解,该沉淀是氯化银;
⑤铝离子能和氢氧化钠反应有白色沉淀生成,氢氧化钠过量时沉淀又完全溶解,氢氧化钠和铵盐加热时反应,生成的气体氨气能使湿润的红色石蕊试纸变蓝.
②溶液少量加新制氯水及CCl4振荡,碘单质能使CCl4层呈紫色;
③加入氯化钡溶液,有白色沉淀生成,加入HNO3后沉淀不溶解,则该白色沉淀是硫酸钡;
④溶液中加入硝酸银溶液有白色沉淀,加入HNO3后沉淀不溶解,该沉淀是氯化银;
⑤铝离子能和氢氧化钠反应有白色沉淀生成,氢氧化钠过量时沉淀又完全溶解,氢氧化钠和铵盐加热时反应,生成的气体氨气能使湿润的红色石蕊试纸变蓝.
解答:
解:①该溶液可使pH试纸呈现红色是酸性溶液,则一定不含有CO32-;
②溶液少量加新制氯水及CCl4振荡,能使CCl4层呈紫色,则生成碘单质,一定含有I-,一定不含有Fe3+、NO3-;
③加入氯化钡溶液,有白色沉淀生成,加入HNO3后沉淀不溶解,则该白色沉淀是硫酸钡,一定含有SO42-,一定不含有Ba2+,;
④溶液中加入硝酸银溶液有白色沉淀,加入HNO3后沉淀不溶解,该沉淀是氯化银,此时的氯离子可能是氯化钡带入的,还有可能原溶液中含有的氯离子,不能确定;
⑤取原溶液少量加入NaOH溶液至碱性,在此过程中有白色沉淀生成,最后沉淀又完全溶解,则一定含有铝离子,没有 Mg2+,加热时反应,有无色气体放出,该气体能使湿润的红色石蕊试纸变蓝,该气体是氨气,一定含NH4+.
故肯定存在的离子有:NH4+、Al3+、I-、SO42-;肯定不存在的离子有:Mg2+、Ba2+、Fe3+、CO32-、NO3-;无法确定是否存在的离子有:K+、Cl-;
故答案为:NH4+、Al3+、I-、SO42-;Mg2+、Ba2+、Fe3+、CO32-、NO3-; K+、Cl-.
②溶液少量加新制氯水及CCl4振荡,能使CCl4层呈紫色,则生成碘单质,一定含有I-,一定不含有Fe3+、NO3-;
③加入氯化钡溶液,有白色沉淀生成,加入HNO3后沉淀不溶解,则该白色沉淀是硫酸钡,一定含有SO42-,一定不含有Ba2+,;
④溶液中加入硝酸银溶液有白色沉淀,加入HNO3后沉淀不溶解,该沉淀是氯化银,此时的氯离子可能是氯化钡带入的,还有可能原溶液中含有的氯离子,不能确定;
⑤取原溶液少量加入NaOH溶液至碱性,在此过程中有白色沉淀生成,最后沉淀又完全溶解,则一定含有铝离子,没有 Mg2+,加热时反应,有无色气体放出,该气体能使湿润的红色石蕊试纸变蓝,该气体是氨气,一定含NH4+.
故肯定存在的离子有:NH4+、Al3+、I-、SO42-;肯定不存在的离子有:Mg2+、Ba2+、Fe3+、CO32-、NO3-;无法确定是否存在的离子有:K+、Cl-;
故答案为:NH4+、Al3+、I-、SO42-;Mg2+、Ba2+、Fe3+、CO32-、NO3-; K+、Cl-.
点评:本题主要考查了根据实验现象判断离子共存,要掌握根据实验现象判断存在的离子,排除与该离子反应的离子.

练习册系列答案
相关题目
用石墨电极电解100mLH2SO4与CuSO4的混合溶液,通电一段时间后,阴、阳极两极分别收集到2.24L和3.36L气体(标准状况),溶液要想恢复电解前的状态可加入下列( )
| A、0.1molCuO |
| B、0.1molCuCO3 |
| C、0.1molCu(OH)2 |
| D、0.1molCu2(OH)2CO3 |
 如图装置,将液体A逐滴加入固体B中,下列叙述正确的是( )
如图装置,将液体A逐滴加入固体B中,下列叙述正确的是( )| A、若A为浓盐酸,B为MnO2,C中盛品红溶液,则C中溶液褪色 |
| B、若A为醋酸,B为贝壳,C中盛澄清石灰水,则C中溶液变浑浊 |
| C、若A为浓氨水,B为生石灰,C中盛A1C13溶液,则C中先产生白色沉淀后沉淀又溶解 |
| D、实验仪器D可以起到防止溶液倒吸的作用 |
下列说法正确的是( )
| A、用10mL量筒量取7.8mL浓H2SO4 |
| B、用碱式滴定管量取18.20mLKMnO4溶液 |
| C、酸碱中和滴定时,滴定管和锥形瓶需分别用标准液和待测液润洗 |
| D、读取标准液读数时,若滴定前仰视,滴定后俯视,会导致测定结果偏低 |
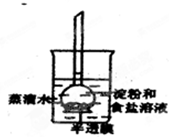 如图所示,烧杯内装有蒸馏水,下部封有半透膜的长颈漏斗内装有淀粉和食盐溶液,漏斗颈内的液面略高于烧杯内蒸馏水的液面,过一段时间后用碘水和硝酸银溶液分别检验蒸馏水中的物质.整个实验过程中,所观察到的现象是( )
如图所示,烧杯内装有蒸馏水,下部封有半透膜的长颈漏斗内装有淀粉和食盐溶液,漏斗颈内的液面略高于烧杯内蒸馏水的液面,过一段时间后用碘水和硝酸银溶液分别检验蒸馏水中的物质.整个实验过程中,所观察到的现象是( )| A、漏斗颈内液面下降 |
| B、漏斗颈内液面上升 |
| C、烧杯内液体遇硝酸银溶液没有白色沉淀生成 |
| D、烧杯内液体遇碘水变蓝 |
下列溶液一定是显酸性的是( )
| A、pH<7的溶液 |
| B、c(H+)>c(OH-)的溶液 |
| C、能与金属Al反应放出H2的溶液 |
| D、滴加酚酞后显无色的溶液 |
 苯和溴取代反应的实验装置如图所示,其中A为由具支试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入少量铁屑粉.填写下列空白:
苯和溴取代反应的实验装置如图所示,其中A为由具支试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入少量铁屑粉.填写下列空白: