题目内容
盛有N2和NO2混合气体25毫升的量筒,倒立于盛有水的水槽中,过一段时间后,气体的体积不再变化,测得气体体积为15毫升,则原混合气体中N2和NO2的体积比是( )
| A、3:2 | B、1:4 |
| C、2:3 | D、3:1 |
考点:化学方程式的有关计算,有关混合物反应的计算
专题:计算题
分析:混合气体倒立水中,发生反应:3NO2+H2O=2HNO3+NO,导致气体体积减小,根据气体体积变化,利用体积差量法计算.
解答:
解:混合气体倒立水中,体积不变时,气体体积减小25mL-15mL=10mL,
3NO2+H2O=2HNO3+NO 体积减小
3 2
V(NO2) 10mL
则V(NO2)=
=15mL
故混合气体中N2的体积为25mL-15mL=10mL,
原混合气体中N2和NO2的体积比是10mL:15mL=2:3,
故选C.
3NO2+H2O=2HNO3+NO 体积减小
3 2
V(NO2) 10mL
则V(NO2)=
| 3×10mL |
| 2 |
故混合气体中N2的体积为25mL-15mL=10mL,
原混合气体中N2和NO2的体积比是10mL:15mL=2:3,
故选C.
点评:本题考查混合物计算,难度不大,明确体积减小的原因是二氧化氮与水反应导致,再根据差量法计算.

练习册系列答案
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案
相关题目
Na2O、NaOH、Na2CO3、NaCl、Na2SO4可按某种标准划分为同一类物质.下列分类标准正确的是( )
①钠的化合物 ②能与硝酸反应的物质 ③电解质 ④钠盐 ⑤钠的含氧化合物.
①钠的化合物 ②能与硝酸反应的物质 ③电解质 ④钠盐 ⑤钠的含氧化合物.
| A、①④ | B、③④ | C、②⑤ | D、①③ |
人体血液的PH为维持在7.35~7.45,适量的CO2对维持这个PH变化范围其主要作用,其原理可用化学方程式表示:H2O+CO2=H++HCO3-.又知人体在正常情况下呼出的气体中CO2的体积分数约为5%,下了说法中正确的是( )
| A、安静状态下,长时间太快且太深的呼吸可以使呼出的气体中CO2的体积分数大于5% |
| B、人在痛苦中,长时间太深的呼吸可导致血液PH降低 |
| C、人在安静状态下,长时间太浅的呼吸可以导致血液PH降低 |
| D、窒息而死的人血液PH高于7.45 |
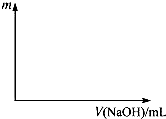 将等物质的量的两种氧化物溶于100mL硫酸,而后逐滴加入1.00mol?L-1的NaOH溶液.当加入的NaOH的体积V1=50mL时,开始有沉淀析出,且沉淀量随NaOH加入量逐渐增加;当NaOH的体积V2=650mL 时,沉淀量达最大值,继续滴加NaOH时,沉淀量逐渐减小;当V3≥750mL时,沉淀量不再改变.
将等物质的量的两种氧化物溶于100mL硫酸,而后逐滴加入1.00mol?L-1的NaOH溶液.当加入的NaOH的体积V1=50mL时,开始有沉淀析出,且沉淀量随NaOH加入量逐渐增加;当NaOH的体积V2=650mL 时,沉淀量达最大值,继续滴加NaOH时,沉淀量逐渐减小;当V3≥750mL时,沉淀量不再改变.