题目内容
6.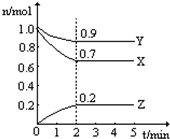 某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据填空:
某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据填空:(1)该反应的化学方程式为Y+3X?2Z.
(2)反应开始至2min末,气体Z的平均反应速率为0.05mol/(L.min).
(3)反应进行到第4min末时,X的转化率为30%.
分析 由图可知,Y、X的物质的量减少,则Y、X为反应物,而Z的物质的量增加,可知Z为生成物,结合v=$\frac{△c}{△t}$、速率之比等于化学计量数之比、转化率=$\frac{转化的量}{开始的量}$×100%来解答.
解答 解:(1)由图可知,Y、X的物质的量减少,则Y、X为反应物,而Z的物质的量增加,可知Z为生成物,v(Y):v(X):v(Z)=△n(Y):△n(X):△n(Z)=(1-0.9):(1-0.7):(0.2-0)=1:3:2,且2min后物质的量不再变化,由速率之比等于化学计量数之比可知反应为Y+3X?2Z,
故答案为:Y+3X?2Z;
(2)反应开始至2min末,气体Z的平均反应速率为$\frac{\frac{0.2mol}{2L}}{2min}$=0.05mol/(L.min),故答案为:0.05mol/(L.min);
(3)2min后物质的量不再变化,反应进行到第4min末时,X的转化率为$\frac{1-0.7}{1}$×100%=30%,故答案为:30%.
点评 本题考查物质的量随时间的变化曲线,为高频考点,把握图象中物质的量的变化、速率计算及速率与化学计量数的关系为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
18.下列物质性质与用途对应关系正确的是( )
| A. | Na2O2具有强的氧化性,可以做供氧剂 | |
| B. | Na2CO3溶液呈碱性,可以清除餐具表面的油污 | |
| C. | 晶体硅熔点高、硬度大,可用于制作半导体材料 | |
| D. | 铜的金属活泼性比铁的差,可在海轮外壳上装若干铜块以减缓其腐蚀 |
14.下列说法正确的是( )
| A. | 酸式盐的溶液一定显碱性 | |
| B. | 只要酸与碱的物质的量浓度和体积分别相等,它们反应后的溶液是中性的 | |
| C. | 纯水呈中性时因为水中c(H+)=c(OHˉ) | |
| D. | 碳酸溶液中氢离子的物质的量浓度是碳酸根离子物质的量浓度的2倍 |
1.往三氯化铁溶液中加入下列溶液后,会出现红褐色沉淀的是( )
| A. | NaOH | B. | BaCl2 | C. | H2SO4 | D. | HNO3 |
18.下列物质中,既含有非极性共价键又含有离子键的是( )
| A. | Na2O2 | B. | NaCl | C. | NaOH | D. | Br2 |
 .
. .
. (2)水
(2)水 (3)氮气
(3)氮气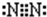 (4)氯化钠
(4)氯化钠
 (6)氢气H:H(7)氯化镁
(6)氢气H:H(7)氯化镁 (8)二氧化碳
(8)二氧化碳 .
.