��Ŀ����
���и���ʵ��������������ó��Ľ�����ȷ����
ѡ�� | ʵ����� | ʵ������ | ���� |
A | ����ľƾ���Һ����һ��������ˮ�е���ɫ��Һ�壬�ü�������� | �ж����ЧӦ | ��ɫҺ��Ϊ���� |
B | ��FeSO4����ǿ�ȣ��ú���ɫ���壬����������ͨ��BaCl2��Һ | ������ɫ���� | ��ɫ����ΪBaSO4��BaSO3 |
C | ������X�ֱ�ͨ��Ʒ����Һ�����Ը��������Һ | ����Һ����ɫ | X��������ϩ |
D | ����ҺY�еμ����ᣬ�ٵμ�BaCl2��Һ | �а�ɫ�������� | Y��һ������SO42- |
 ��ս�п�����ϵ�д�
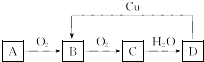
��ս�п�����ϵ�д�| A�� | ���� | B�� | ���ȼ��� | C�� | ���ȼ��� | D�� | ���� |
����Cu2O���ھ��������Ĵ����ܶ��ܵ���ע���±�Ϊ��ȡCu2O�����ַ�����
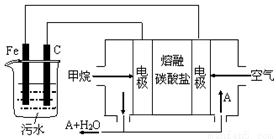
����I | ��̼���ڸ��������»�ԭCuO |
����II | ���£�N2H4����ԭ����Cu��OH��2 |
����III | ��ⷨ����ӦΪ2Cu+H2O |
��1����֪��2Cu��s��+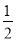 O2��g��=Cu2O��s����H=��akJ•mol��1
O2��g��=Cu2O��s����H=��akJ•mol��1
C��s��+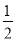 O2��g��=CO��g����H=��bkJ•mol��1
O2��g��=CO��g����H=��bkJ•mol��1
Cu��s��+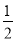 O2��g��=CuO��s����H=��ckJ•mol��1
O2��g��=CuO��s����H=��ckJ•mol��1
��I�����ķ�Ӧ��2Cu O��s��+C��s��=Cu2O��s��+CO��g������H= kJ•mol��1��
��2����ҵ�Ϻ����÷���I��ȡCu2O�������ڷ���I��Ӧ���������ƣ������²������ή��Cu2O���ʣ������ԭ�� ��
��3������IIΪ������������Һ̬�£�N2H4����ԭ����Cu��OH��2���Ʊ�����Cu2O��ͬʱ�ų�N2��
���Ʒ��Ļ�ѧ����ʽΪ ��
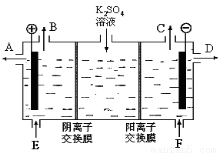
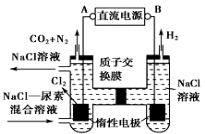
��4������III�������ӽ���Ĥ���Ƶ��Һ��OH����Ũ�ȶ��Ʊ�����Cu2O��װ����ͼ��ʾ��д���缫��Ӧʽ
��˵����װ���Ʊ�Cu2O��ԭ�� ��
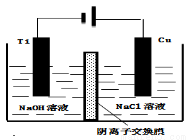
��5������ͬ���ܱ������У����������ַ����Ƶõ�Cu2O�ֱ���д��ֽ�ˮ��ʵ�飺
2H2O��g��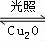 2H2��g��+O2��g����H��0��ˮ������Ũ�ȣ�mol/L����ʱ��t��min��
2H2��g��+O2��g����H��0��ˮ������Ũ�ȣ�mol/L����ʱ��t��min��
�仯���±���ʾ��
��� | Cu2O a�� | �¶� | 0 | 10 | 20 | 30 | 40 | 50 |
�� | ����II | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
�� | ����III | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
�� | ����III | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
����������ȷ���� ������ĸ���ţ���
a��ʵ����¶ȣ�T2��T1
b��ʵ���ǰ20min��ƽ����Ӧ����v��O2��=7��10��5mol•L��1•min��1
c��ʵ��ڱ�ʵ������õ�Cu2O��Ч�ʸ�
d�� ʵ��١��ڡ��۵Ļ�ѧƽ�ⳣ���Ĺ�ϵ��K1=K2��K3��
��A��B�����ܱ������У���һ�������·�����Ӧ��A(g)+B(s) 2C(g)�����Թ��������ƽ��ʱC���������
2C(g)�����Թ��������ƽ��ʱC��������� (%)���¶Ⱥ�ѹǿ�ı仯���±���ʾ��
(%)���¶Ⱥ�ѹǿ�ı仯���±���ʾ��
ѹǿ/MPa �������/% �¶�/�� | 1.0 | 2.0 | 3.0 |
800 | 54.0 | a | b |
900 | c | 75.0 | d |
1000 | e | f | 83.0 |
��a��b �ڸ÷�Ӧ���ر��S��0 ��900�桢2.0MPaʱA��ת����Ϊ60%
��K(1000��)��K(800��) ������ӦΪ���ȷ�Ӧ �����١�������ȷ����( )
A.4�� B.3�� C.2�� D.1��


 Cu2O+H2��
Cu2O+H2��

 ����Ӧ��2Cl--2e-=Cl2��
����Ӧ��2Cl--2e-=Cl2��