题目内容
硫酸工业中废渣的成分为SiO2、Fe2O3、Al2O3、MgO. 某探究性学习小组的同学设计以下实验方案,将硫酸渣中金属元素转化为氢氧化物沉淀分离开来.
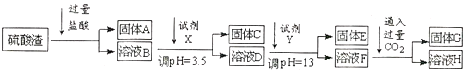
已知常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
(1)工业上用固体A作原料制取粗硅的化学方程式为 .
(2)实验室用11.9mol/L的浓盐酸配制250mL3.0mol/L的稀盐酸,所用的玻璃仪器除烧杯、玻璃棒和量筒外,还需要 .
(3)上述流程中的试剂Y最好选用下列中的 (选填字母编号).
A.水 B.氧化镁 C.氨水 D.氢氧化钠
(4)写出反应F→H的离子方程式 .
(5)溶液H显碱性,原因是 (用离子方程式和必要的文字说明).
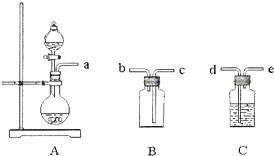
(6)实验室可用大理石和稀盐酸反应制取上述流程中所需的CO2,仪器如下,装置A产生CO2,按气流方向连接各仪器接口,顺序为a→ ,装置C中应 盛放的试剂为 .

已知常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
| 阳离子 | Fe3+ | Al3+ | Mg2+ |
| 开始沉淀时的pH | 1.9 | 3.7 | 9.6 |
| 沉淀完全时的pH | 3.2 | 5.2 | 11.0 |
(2)实验室用11.9mol/L的浓盐酸配制250mL3.0mol/L的稀盐酸,所用的玻璃仪器除烧杯、玻璃棒和量筒外,还需要
(3)上述流程中的试剂Y最好选用下列中的
A.水 B.氧化镁 C.氨水 D.氢氧化钠
(4)写出反应F→H的离子方程式
(5)溶液H显碱性,原因是
(6)实验室可用大理石和稀盐酸反应制取上述流程中所需的CO2,仪器如下,装置A产生CO2,按气流方向连接各仪器接口,顺序为a→

考点:金属的回收与环境、资源保护,盐类水解的应用,难溶电解质的溶解平衡及沉淀转化的本质,常见气体制备原理及装置选择,配制一定物质的量浓度的溶液
专题:实验题
分析:(1)以粗硅的制取为背景,考查学生捕捉、获取情境信息的能力,结合所学知识可知利用焦炭还原二氧化硅来制取粗硅.要求学生掌握硅的相关性质,正确书写焦炭与二氧化硅反应的方程式;
(2)掌握一定物质的量浓度溶液的配制实验.考查一定物质的量浓度溶液的配制所需仪器的选择,除题中所给仪器外,还需250mL容量瓶和胶头滴管;
(3)依据阳离子Mg2+以氢氧化物形式沉淀所需试剂的选择,根据题给信息和流程可知应该先用氢氧化钠液将Mg2+转化成氢氧化镁沉淀析出同时将Al3+转化成AlO2-;
(4)AlO2-与CO2 反应离子方程式的书写,清楚过量CO2反应的产物为碳酸氢盐,正确书写离子方程式;
(5)依据NaHCO3溶液显碱性的原因分析,溶液中存在水解平衡,也存在电离平衡,NaHCO3溶液之所以显碱性是因为HCO3-水解程度大于电离程度;
(6)依据CO2气体的实验室制备、除杂、收集方法.学生需根据实验室制备CO2的原理将所给仪器进行合理地组装.利用大理石和稀盐酸本来反应得到的CO2气体中会混有HCl气体气质,应通过盛有饱和NaHCO3溶液的洗气瓶来除去;CO2气体密度大于空气,应采用向上排空气法集.
(2)掌握一定物质的量浓度溶液的配制实验.考查一定物质的量浓度溶液的配制所需仪器的选择,除题中所给仪器外,还需250mL容量瓶和胶头滴管;
(3)依据阳离子Mg2+以氢氧化物形式沉淀所需试剂的选择,根据题给信息和流程可知应该先用氢氧化钠液将Mg2+转化成氢氧化镁沉淀析出同时将Al3+转化成AlO2-;
(4)AlO2-与CO2 反应离子方程式的书写,清楚过量CO2反应的产物为碳酸氢盐,正确书写离子方程式;
(5)依据NaHCO3溶液显碱性的原因分析,溶液中存在水解平衡,也存在电离平衡,NaHCO3溶液之所以显碱性是因为HCO3-水解程度大于电离程度;
(6)依据CO2气体的实验室制备、除杂、收集方法.学生需根据实验室制备CO2的原理将所给仪器进行合理地组装.利用大理石和稀盐酸本来反应得到的CO2气体中会混有HCl气体气质,应通过盛有饱和NaHCO3溶液的洗气瓶来除去;CO2气体密度大于空气,应采用向上排空气法集.
解答:
解:(1)以粗硅的制取为背景,考查学生捕捉、获取情境信息的能力,结合所学知识可知利用焦炭还原二氧化硅来制取粗硅.要求学生掌握硅的相关性质,正确书写焦炭与二氧化硅反应的方程式为:2C+SiO2
Si+2CO↑;
故答案为:2C+SiO2
Si+2CO↑;
(2)实验室用11.9mol/L的浓盐酸配制250mL3.0mol/L的稀盐酸,要求掌握一定物质的量浓度溶液的配制实验.所用的玻璃仪器除烧杯、玻璃棒和量筒外,还需要250mL容量瓶和胶头滴管;
故答案为:250mL容量瓶、胶头滴管;
(3)阳离子Mg2+以氢氧化物形式沉淀所需试剂,根据题给信息和流程可知应该先用氢氧化钠溶液将Mg2+转化成氢氧化镁沉淀析出同时将Al3+转化成AlO2-溶液;
故答案为:D;
(4)F→H的反应是AlO2-与CO2 反应,过量CO2反应的产物为碳酸氢盐,反应的离子方程式:AlO2-+2H2O+CO2=Al(OH)3↓+HCO3-;
故答案为:AlO2-+2H2O+CO2=Al(OH)3↓+HCO3-;
(5)溶液H为NaHCO3溶液,显碱性的原因是因为存在水解平衡,也存在电离平衡,HCO3-?CO32-+H+,HCO3-+H2O?H2CO3+OH-,NaHCO3溶液之所以显碱性是因为HCO3-水解程度大于电离程度;
故答案为:HCO3-?CO32-+H+,HCO3-+H2O?H2CO3+OH-,HCO3-的水解程度大于电离程度;
(6)利用大理石和稀盐酸反应得到的CO2气体中会混有HCl气体气质,应通过盛有饱和NaHCO3溶液的洗气瓶来除去;CO2气体密度大于空气,应采用向上排空气法集,实验室可用大理石和稀盐酸反应制取上述流程中所需的CO2,仪器如下,装置A产生CO2,按气流方向连接各仪器接口,顺序为a→d→e→c→b;
故答案为:d→e→c→b;饱和NaHCO3溶液.
| ||
故答案为:2C+SiO2
| ||
(2)实验室用11.9mol/L的浓盐酸配制250mL3.0mol/L的稀盐酸,要求掌握一定物质的量浓度溶液的配制实验.所用的玻璃仪器除烧杯、玻璃棒和量筒外,还需要250mL容量瓶和胶头滴管;
故答案为:250mL容量瓶、胶头滴管;
(3)阳离子Mg2+以氢氧化物形式沉淀所需试剂,根据题给信息和流程可知应该先用氢氧化钠溶液将Mg2+转化成氢氧化镁沉淀析出同时将Al3+转化成AlO2-溶液;
故答案为:D;
(4)F→H的反应是AlO2-与CO2 反应,过量CO2反应的产物为碳酸氢盐,反应的离子方程式:AlO2-+2H2O+CO2=Al(OH)3↓+HCO3-;
故答案为:AlO2-+2H2O+CO2=Al(OH)3↓+HCO3-;
(5)溶液H为NaHCO3溶液,显碱性的原因是因为存在水解平衡,也存在电离平衡,HCO3-?CO32-+H+,HCO3-+H2O?H2CO3+OH-,NaHCO3溶液之所以显碱性是因为HCO3-水解程度大于电离程度;
故答案为:HCO3-?CO32-+H+,HCO3-+H2O?H2CO3+OH-,HCO3-的水解程度大于电离程度;
(6)利用大理石和稀盐酸反应得到的CO2气体中会混有HCl气体气质,应通过盛有饱和NaHCO3溶液的洗气瓶来除去;CO2气体密度大于空气,应采用向上排空气法集,实验室可用大理石和稀盐酸反应制取上述流程中所需的CO2,仪器如下,装置A产生CO2,按气流方向连接各仪器接口,顺序为a→d→e→c→b;
故答案为:d→e→c→b;饱和NaHCO3溶液.
点评:本题考查了溶液配制实验过程和仪器选择,盐类水解应用,掌握物质性质和实验流程分析是解题关键,题目难度中等.

练习册系列答案
相关题目
钠的下列性质中,和钠与水反应的现象无关的是( )
| A、钠的熔点低 |
| B、钠的密度小 |
| C、钠的硬度小 |
| D、钠有强还原性 |
M(NO3)2热分解化学方程式为:2M(NO3)2
2MO+4NO2↑+O2↑,加热29.6g M(NO3)2使其完全分解,在标准状况下收集11200mL的气体,那么M的摩尔质量是( )
| ||
| A、64g/mol |
| B、24g/mol |
| C、65g/mol |
| D、40g/mol |
C、N、S都是重要的非金属元素.下列说法正确的是( )
| A、三者对应的氧化物均为酸性氧化物 |
| B、实验室可用NaOH溶液处理SO2、NO2 |
| C、CO2、NO2、SO2都能与H2O反应,其反应原理相同 |
| D、三者的单质直接与氧气反应都能生成两种氧化物 |
下列有关工业生产的叙述正确的是( )
| A、合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2?H2的转化率 |
| B、工业上利用电解熔融的氧化铝制取铝,电解熔融的氧化镁制取镁 |
| C、电解精炼铜时,同一时间内阴极溶解铜的质量比阳极析出铜的质量小 |
| D、从海带中提取碘单质的实验中,要经过煅烧、溶解、过滤和萃取等操作 |